题目内容
【题目】已知反应:10AgF+5Cl2+5H2O=9AgCl+AgClO3+10HF+O2,试回答:
(1)反应中氧化剂和还原剂的物质的量之比是_____;
(2)当转移1 mol电子时,被氧化的Cl2的物质的量是___;
(3)每产生1 mol O2时,被氧元素还原的Cl2的物质的量是_____;
(4)反应消耗的水是(_____)
A.全部被氧化 B.全部被还原 C.![]() 被氧化 D.
被氧化 D.![]() 被还原
被还原
【答案】9:5 1/18 2mol C
【解析】
反应10AgF+5Cl2+5H2O═9AgCl+AgClO3+10HF+O2中,Cl元素的化合价既升高又降低,其中9molCl原子得电子,1molCl原子失电子,O元素的化合价升高,2molO原子失电子,以此来解答。
(1)反应10AgF+5Cl2+5H2O═9AgCl+AgClO3+10HF+O2中,9 mol Cl原子得电子,1 mol Cl原子失电子,2 mol O原子失电子,则氧化剂为4.5 mol,还原剂物质的量为0.5mol+2mol=2.5 mol,所以氧化剂与还原剂物质的量之比为9:5,故答案为:9:5;
(2)反应10AgF+5Cl2+5H2O═9AgCl+AgClO3+10HF+O2中,5mol氯气反应时,被氧化的氯气为0.5 mol,转移电子的物质的量为9 mol,则当转移1mol电子时,被氧化的Cl2的物质的量是1/18mol,故答案为:1/18;
(3)每产生1 mol O2时,O元素失去4 mol电子,则氯元素得到4 mol,所以被氧元素还原的氯气物质的量为2 mol,故答案为:2mol;
(4)由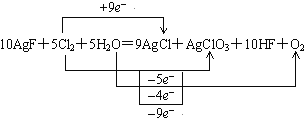 可知,5 mol H2O参加反应,只有2 mol作还原剂被氧化,即反应消耗的水是
可知,5 mol H2O参加反应,只有2 mol作还原剂被氧化,即反应消耗的水是![]() 被氧化,C项正确,故答案为:C。
被氧化,C项正确,故答案为:C。

 期末宝典单元检测分类复习卷系列答案
期末宝典单元检测分类复习卷系列答案【题目】在呼吸面具和潜水艇中可用过氧化钠作为供氧剂,请选择适当的化学试剂和实验用品,用下图中的实验装置进行实验,证明过氧化钠可作供氧剂。

(1)A是制取CO2的装置.写出A中发生反应的化学方程式___________________。
(2)填写表中空格:
仪器 | 加入试剂 | 加入该试剂的目的 |
B | 饱和NaHCO3溶液 | 除去二氧化碳中的氯化氢 |
C | ____________ | ____________ |
D | NaOH溶液 | ____________ |
(3)写出C中发生反应的化学方程式:___________________。
(4)试管F中收集满气体后,下一步实验操作是把E中的导管移出水面,关闭分液漏斗活塞,用拇指堵住试管口,取出试管,立即把_____________________,则证明试管中收集的气体是氧气。
【题目】在一定条件下,将A和B各0.32mol充入10L恒容密闭容器中,发生反应:
A(g)+B(g)![]() 2C(g) △H<0,反应过程中测定的数据如下表,下列说法正确的是
2C(g) △H<0,反应过程中测定的数据如下表,下列说法正确的是
t/min | 0 | 2 | 4 | 7 | 9 |
n(B)/mol | 0.32 | 0.24 | 0.22 | 0.20 | 0.20 |
A. 反应前2 min的平均速率v(C)=0.004 mol/(L·min)
B. 其他条件不变,降低温度,反应达到新平衡前v (逆)> v (正)
C. 其他条件不变,起始时向容器中充入0.64mol A和0.64mol B,平衡时n(C)<0.48mol
D. 其他条件不变,向平衡体系中再充入0.32mol A,再次平衡时,B的转化率增大
【题目】甲醇可作为燃料电池的原料。工业上利用CO2和H2在一定条件下反应合成甲醇。
(1)已知在常温常压下:
① 2CH3OH(l)+3O2(g) ===2CO2(g)+4H2O(g) ΔH=-1275.6 kJ/mol
② 2CO (g)+ O2(g) === 2CO2(g) ΔH=-566.0 kJ/mol
③ H2O(g) ===H2O(l) ΔH=-44.0 kJ/mol
写出甲醇不完全燃烧生成一氧化碳和液态水的热化学方程式:______________
(2)甲醇脱氢可制取甲醛CH3OH(g)![]() HCHO(g)+H2(g),甲醇的平衡转化率随温度变化曲线如下图所示。回答下列问题:
HCHO(g)+H2(g),甲醇的平衡转化率随温度变化曲线如下图所示。回答下列问题:

①600K时,Y点甲醇的υ(逆)_____υ(正)(填“>”或“<”)
②若改变条件使之从Y点到X点,则改变条件可以是___________。
(3)纳米级Cu2O由于具有优良的催化性能而受到关注。在相同的密闭容器中,使用不同方法制得的Cu2O(I)和(II)分别进行催化CH3OH的脱氢实验:CH3OH(g)![]() HCHO(g)+H2(g),CH3OH的浓度(mol·L-1)随时间t (min)变化如下表:
HCHO(g)+H2(g),CH3OH的浓度(mol·L-1)随时间t (min)变化如下表:
序号 | 温度 | 0 | 10 | 20 | 30 | 40 | 50 |
① | T1 | 0.050 | 0.0492 | 0.0486 | 0.0482 | 0.0480 | 0.0480 |
② | T1 | 0.050 | 0.0488 | 0.0484 | 0.0480 | 0.0480 | 0.0480 |
③ | T2 | 0.10 | 0.094 | 0.090 | 0.090 | 0.090 | 0.090 |
可以判断:实验①的前20 min的平均反应速率 ν(H2)=________;实验温度T1_____T2(填“>”、“<”);催化剂的催化效率:实验①________实验②(填“>”、“<”)。
(4)电解法可消除甲醇对水质造成的污染,原理是:通电将Co2+氧化成Co3+,然后Co3+将甲醇氧化成CO2和H+(用石墨烯吸附除去Co2+)。现用如下图所示装置模拟上述过程, 除去甲醇的离子方程式为____________


