题目内容
取两种不同浓度的NaOH溶液各100 ml,分别向两种溶液中通入标准状况下CO2 1.12 L,完全反应后,将溶液低温下蒸干分别得到不含结晶水的固体5 g和6 g,求两种NaOH溶液的物质的量浓度。
答案:
解析:
提示:
解析:
(1)5 g固体的组成为:Na2CO3和NaHCO3。c(NaOH)=0.864 mol·L-1 (2)6 g固体的组成为:NaOH和Na2CO3。c(NaOH)=1.18 mol·L-1
|
提示:
此题的关键是确定最后固体的组成,固体组成可能为: A.NaOH和Na2CO3 B.Na2CO3 C.Na2CO3和NaHCO3 D.NaHCO3 不管是哪一种,都含碳原子,且碳原子来源于CO2,碳原子的物质的量,即CO2的物质的量为:1.12 L/22.4 L·mol-1=0.05 mol 若0.05 mol CO2全变为Na2CO3,其质量应为5.3 g;若0.05 mol CO2全变为NaHCO3,其质量应为4.2 g。 由此可得:5 g固体的组成为Na2CO3和NaHCO3。再根据化学方程式计算可得c(NaOH)=0.864 mol·L-1; 6 g固体的组成为:NaOH和Na2CO3。再根据化学方程式计算可得c(NaOH)=1.18 mol·L-1
|

练习册系列答案
相关题目
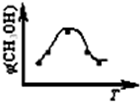 (2012?丹东模拟)能源短缺是人类面临的重大问题.甲醇是一种可再生能源.具有广泛的开发和应用前景.因此甲醇被称为21世纪的新型燃料.
(2012?丹东模拟)能源短缺是人类面临的重大问题.甲醇是一种可再生能源.具有广泛的开发和应用前景.因此甲醇被称为21世纪的新型燃料. A、B、C、X是中学化学常见物质,均由短周期元素组成,转化关系如图所示.请针对以下不同情况回答:
A、B、C、X是中学化学常见物质,均由短周期元素组成,转化关系如图所示.请针对以下不同情况回答: Ⅰ.研究NO2、SO2、CO等大气污染气体的处理具有重要意义.
Ⅰ.研究NO2、SO2、CO等大气污染气体的处理具有重要意义.