题目内容
(8分)已知A、B、C、D、E、F、G都是中学化学常见的物质,下图中A为淡黄色固体,
B、C为溶液,D、G为无色气体,E、F为白色沉淀。
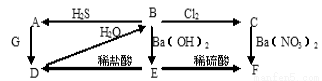
①写出B→C的离子方程式
②写出D和G反应的化学方程式
③写出过量的D通入Ba(OH)2溶液中的离子方程式
④从上图出现的物质中选出反应物,写出一个置换反应,以验证氯元素原子的氧化性比硫元素原子的氧化性强
(1)H2SO3+Cl2= 4H++SO42-+2Cl- ; (2)  ;
;
(3)OH- + SO2 = HSO3-;(4)H2S + Cl2 =S + 2HCl。
【解析】
试题分析:根据题意及物质之间转化关系图示可知:A是S;B是H2SO3;C是H2SO4;D是SO2;E是BaSO3;F是BaSO4,G是O2。①写出B→C的离子方程式是H2SO3+Cl2= 4H++SO42-+2Cl- ; ②D和G反应的化学方程式是 ;③当SO2过量时会形成酸式盐亚硫酸氢钡,反应的离子方程式是OH- + SO2 = HSO3-;④验证氯元素原子的氧化性比硫元素原子的氧化性强一个置换反应,是H2S + Cl2 =S + 2HCl。
;③当SO2过量时会形成酸式盐亚硫酸氢钡,反应的离子方程式是OH- + SO2 = HSO3-;④验证氯元素原子的氧化性比硫元素原子的氧化性强一个置换反应,是H2S + Cl2 =S + 2HCl。
考点:考查元素及化合物的推断、化学方程式、离子方程式的书写的知识。

练习册系列答案
 一线名师提优试卷系列答案
一线名师提优试卷系列答案 阳光试卷单元测试卷系列答案
阳光试卷单元测试卷系列答案
相关题目
 2
2 /L Na2CO3 溶液中,逐滴加入1
/L Na2CO3 溶液中,逐滴加入1 75
75

 表示的有机物中,能发生消去反应的共有
表示的有机物中,能发生消去反应的共有