题目内容
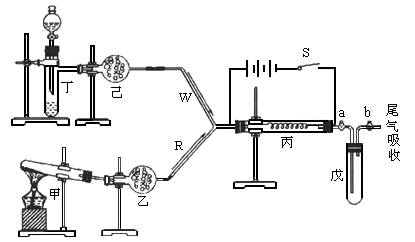
实验室用下列装置所示的流程进行气体性质实验。图中用箭头表示气体的流向,A为一种纯净、干燥的气体,B是另一种气体,己中有红棕色气体出现。实验中所用的药品只能从下列物质中选取:Na2CO3、NaHCO3、Na2O、Na2O2、NaCl、无水CaCl2、(NH4)2CO3、碱石灰等固体和蒸馏水。
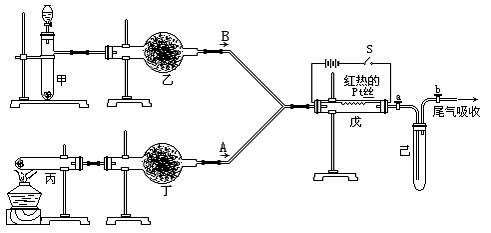
根据图中装置和现象回答:
(1)丙中发生反应的化学方程式为___________________________________。
(2)丁中应选用的干燥剂是_________,为什么不选用所给的另一种干燥剂______________。
(3)甲中发生反应的化学方程式___________________________。
(4)戊中发生的主要反应的化学方程式______________________。此反应是吸热反应还是放热反应___________,估计可看到什么现象足以说明你的判断_________________。
(5)当己中充满红棕色气体后,停止给丙加热并关闭a、b两个活塞。若将己浸入冰水中,则己中将有什么现象发生?简述发生此现象的原因____________________________。
(1)(NH4)2CO3![]() 2NH3↑+CO2↑+H2O
2NH3↑+CO2↑+H2O
(2)碱石灰 因为另一种干燥剂的无水CaCl2,只能吸收水,不能吸收CO2,不能使氨气完全净化。
(3)2Na2O2+2H2O = 4NaOH+O2↑
(4)4NH3+5O2 ![]() 4NO+6H2O放热,可以看到戊中铂丝比开始反应时更加红热
4NO+6H2O放热,可以看到戊中铂丝比开始反应时更加红热
(5)己中的红棕色气体颜色变浅,因为当己浸入冰水中时,温度下降,红棕色的NO2
能转化成无色的N2O4,2NO2![]() N2O4+Q。降低温度时平衡向右移动,c(NO2)减小,c(N2O4)增大,所以颜色变浅。
N2O4+Q。降低温度时平衡向右移动,c(NO2)减小,c(N2O4)增大,所以颜色变浅。



 CH3COONH4+H2O+2Ag↓+3NH3
CH3COONH4+H2O+2Ag↓+3NH3
 下列有关实验原理或实验操作正确的是( )
下列有关实验原理或实验操作正确的是( )