题目内容
1.将30mL 1mol/L NaOH溶液加水稀释到500mL,稀释后溶液中NaOH的物质的量浓度为( )| A. | 0.03 mol/L | B. | 0.04 mol/L | C. | 0.05 mol/L | D. | 0.06mol/L |
分析 稀释过程中溶质氢氧化钠的物质的量不变,根据c=$\frac{n}{V}$计算出稀释后溶液中氢氧化钠的物质的量浓度.
解答 解:稀释过程中溶质NaOH的物质的量不变,
则稀释后溶液中氢氧化钠的浓度为:c=$\frac{1mol/L×0.03L}{0.5L}$=0.06mol/L,
故选D.
点评 本题考查了物质的量浓度的计算,题目难度不大,明确溶液稀释过程中溶质的物质的量不变为解答关键,注意掌握物质的量浓度的概念及表达式,试题培养了学生的学生的化学计算能力.

练习册系列答案
 龙人图书快乐假期暑假作业郑州大学出版社系列答案
龙人图书快乐假期暑假作业郑州大学出版社系列答案
相关题目
11.下列各组分子中,都属于含有极性键的非极性分子的一组是( )
| A. | CO2H2O | B. | C2H4 CH4 | C. | Cl2 C2H2 | D. | NH3HCl |
9.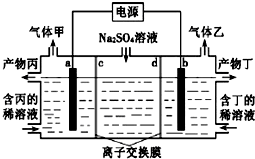 电解硫酸钠溶液联合生产硫酸和烧碱溶液的装置如图所示,其中阴极和阳极均为惰性电极.测得同温同压下,气体甲与气体乙的体积比约为1:2,以下说法不正确的是( )
电解硫酸钠溶液联合生产硫酸和烧碱溶液的装置如图所示,其中阴极和阳极均为惰性电极.测得同温同压下,气体甲与气体乙的体积比约为1:2,以下说法不正确的是( )
 电解硫酸钠溶液联合生产硫酸和烧碱溶液的装置如图所示,其中阴极和阳极均为惰性电极.测得同温同压下,气体甲与气体乙的体积比约为1:2,以下说法不正确的是( )
电解硫酸钠溶液联合生产硫酸和烧碱溶液的装置如图所示,其中阴极和阳极均为惰性电极.测得同温同压下,气体甲与气体乙的体积比约为1:2,以下说法不正确的是( )| A. | a极与电源的正极相连 | |
| B. | 产物丙为硫酸溶液 | |
| C. | 离子交换膜d为阳离子交换膜(允许阳离子通过) | |
| D. | a电极反应式为2H2O+2e-═2OH-+H2↑ |
6.某溶液中加入KSCN溶液无明显现象,再通入氯气,溶液立即变为红色,说明原溶液中一定含有( )
| A. | Fe3+ | B. | Fe2+ | C. | Cu2+ | D. | Zn2+ |
10.在一定的温度下,下列叙述与图象对应正确的是( )
| A. |  曲线可表示向0.1 mol/L CH3COONa溶液中加水稀释的过程中OH-浓度随溶液体积的变化趋势 | |
| B. | 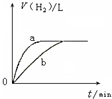 曲线a、b分别表示过量纯锌、过量粗锌(含Cu、C杂质)跟同浓度等体积盐酸反应过程中产生H2体积的变化趋势 | |
| C. |  曲线c、d分别表示等质量的铝分别跟过量烧碱溶液、过量盐酸反应过程中产生H2体积的变化趋势 | |
| D. | 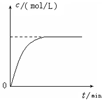 曲线可表示足量锌与一定量稀醋酸反应过程中,Zn2+浓度的变化趋势(假设反应过程中溶液体积保持不变) |
11.下列各组离子能大量共存的是( )
| A. | H+、OH-、SO42- | B. | K+、Mg2+,Cl- | ||
| C. | Ca2+,CO32-,OH- | D. | Ba2+,CO32-,SO42- |
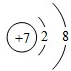 可知,氮原子最外层电子数目为5
可知,氮原子最外层电子数目为5