题目内容
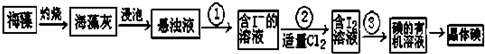
A、B、C是中学化学常见的三种物质,它们之间的相互转化关系如图1(部分反应条件及产物略去).

(1)若A是一种黄色单质固体,则B→C的化学方程式为 .
(2)若A是一种活泼金属,C是淡黄色固体,则C的名称为 ,用化学方程式表示该物质与水的反应 .将C长期露置于空气中,最后将变成物质D,D的化学式为 .现在有D和NaHCO3的固体混合物10g,加热至质量不再改变,剩余固体质量为9.38g,D的质量分数为 .
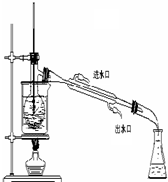
(3)若C是红棕色气体.图2是实验室制取A气体的装置:
①写出实验室制取A的化学方程式 .
②上图中干燥管内可能盛放的物质是 .
a.浓硫酸 b.生石灰 c.碱石灰 d.熟石灰
③为了检验氨气是否集满,可将 ,则证明已收集满.

(1)若A是一种黄色单质固体,则B→C的化学方程式为
(2)若A是一种活泼金属,C是淡黄色固体,则C的名称为
(3)若C是红棕色气体.图2是实验室制取A气体的装置:
①写出实验室制取A的化学方程式
②上图中干燥管内可能盛放的物质是
a.浓硫酸 b.生石灰 c.碱石灰 d.熟石灰
③为了检验氨气是否集满,可将
考点:无机物的推断
专题:推断题
分析:(1)A能连续被氧化,且A是黄色单质固体,则A是S单质,硫和氧气反应生成二氧化硫,二氧化硫被氧气氧化生成三氧化硫;
(2)若A是一种活泼金属,C是淡黄色固体,则A是Na、B是Na2O、C是Na2O2;过氧化钠能和水、二氧化碳反应生成氧气;
(3)若C是红棕色气体,则C是NO2、B是NO,图2装置是实验室制取氨气,A是NH3,
①氯化铵和氢氧化钙在加热条件下反应生成氨气;
②氨气属于碱性气体,应该用碱性或中性物质干燥;
③氨气能使湿润的红色石蕊试纸变蓝色.
(2)若A是一种活泼金属,C是淡黄色固体,则A是Na、B是Na2O、C是Na2O2;过氧化钠能和水、二氧化碳反应生成氧气;
(3)若C是红棕色气体,则C是NO2、B是NO,图2装置是实验室制取氨气,A是NH3,
①氯化铵和氢氧化钙在加热条件下反应生成氨气;
②氨气属于碱性气体,应该用碱性或中性物质干燥;
③氨气能使湿润的红色石蕊试纸变蓝色.
解答:
解:(1)A能连续被氧化,且A是黄色单质固体,则A是S单质,硫和氧气反应生成二氧化硫,二氧化硫被氧气氧化生成三氧化硫,二氧化硫生成三氧化硫方程式为:2SO2+O2
2SO3,故答案为:2SO2+O2
2SO3;
(2)若A是一种活泼金属,C是淡黄色固体,则A是Na、B是Na2O、C是Na2O2,
C的名称为过氧化钠,过氧化钠和水反应生成氢氧化钠和氧气,反应方程式为:2Na2O2+2H2O═4NaOH+O2↑,将过氧化钠长期露置于空气中,过氧化钠和水反应生成NaOH,NaOH和二氧化碳反应生成碳酸钠,过氧化钠和二氧化碳反应生成碳酸钠,所以最后将变成物质D,D的化学式为Na2CO3;
加热时,固体减少的质量是二氧化碳和水,设碳酸钠的质量是x,则碳酸氢钠的质量是(10-x)g,
2NaHCO3
Na2CO3+CO2↑+H2O 固体减少质量
168g 62g
(10-x)g (10-9.38)g
168g:62g=(10-x)g:(10-9.38)g
x=10-
=8.32g,
则碳酸钠的质量分数=
×100%=83.2%;
故答案为:过氧化钠;2Na2O2+2H2O═4NaOH+O2↑;Na2CO3;83.2%;
(3)若C是红棕色气体,则C是NO2、B是NO,图2装置是实验室制取氨气,A是NH3,
①氯化铵和氢氧化钙在加热条件下反应生成氨气,反应方程式为:Ca(OH)2+2NH4Cl
CaCl2+2NH3↑+2H2O,故答案为:Ca(OH)2+2NH4Cl
CaCl2+2NH3↑+2H2O;
②氨气属于碱性气体,应该用碱性或中性物质干燥,所以干燥管内的干燥剂是碱石灰,故选C;
③氨气能使湿润的红色石蕊试纸变蓝色,其检验方法是将湿润的红色石蕊试纸放于试管口,变蓝(或将沾有浓盐酸的玻璃棒放于试管口,产生白烟),
故答案为:将湿润的红色石蕊试纸放于试管口,变蓝(或将沾有浓盐酸的玻璃棒放于试管口,产生白烟).
| ||
| △ |
| ||
| △ |
(2)若A是一种活泼金属,C是淡黄色固体,则A是Na、B是Na2O、C是Na2O2,
C的名称为过氧化钠,过氧化钠和水反应生成氢氧化钠和氧气,反应方程式为:2Na2O2+2H2O═4NaOH+O2↑,将过氧化钠长期露置于空气中,过氧化钠和水反应生成NaOH,NaOH和二氧化碳反应生成碳酸钠,过氧化钠和二氧化碳反应生成碳酸钠,所以最后将变成物质D,D的化学式为Na2CO3;
加热时,固体减少的质量是二氧化碳和水,设碳酸钠的质量是x,则碳酸氢钠的质量是(10-x)g,
2NaHCO3
| ||
168g 62g
(10-x)g (10-9.38)g
168g:62g=(10-x)g:(10-9.38)g
x=10-
| (10-9.38)g×168g |
| 62g |
则碳酸钠的质量分数=
| 8.32g |
| 10g |
故答案为:过氧化钠;2Na2O2+2H2O═4NaOH+O2↑;Na2CO3;83.2%;
(3)若C是红棕色气体,则C是NO2、B是NO,图2装置是实验室制取氨气,A是NH3,
①氯化铵和氢氧化钙在加热条件下反应生成氨气,反应方程式为:Ca(OH)2+2NH4Cl
| ||
| ||
②氨气属于碱性气体,应该用碱性或中性物质干燥,所以干燥管内的干燥剂是碱石灰,故选C;
③氨气能使湿润的红色石蕊试纸变蓝色,其检验方法是将湿润的红色石蕊试纸放于试管口,变蓝(或将沾有浓盐酸的玻璃棒放于试管口,产生白烟),
故答案为:将湿润的红色石蕊试纸放于试管口,变蓝(或将沾有浓盐酸的玻璃棒放于试管口,产生白烟).
点评:本题考查了无机物推断,涉及钠及其化合物、N元素及其化合物、S及其化合物的推断,根据物质的性质来分析解答,知道实验室制取、干燥和收集、检验原理,这些考点都考试热点,明确氨气、铵根离子的检验方法,题目难度中等.

练习册系列答案
相关题目
3Cu+8HNO3(稀)=3Cu(NO3)2+2NO↑+4H2O下列有关说法中不正确的是( )
| A、HNO3在反应中既表现氧化性也表现出酸性 |
| B、每生成22.4L NO(标准状况)有3mol电子转移 |
| C、HNO3作氧化剂,铜作还原剂,3mol Cu还原8mol的HNO3 |
| D、HNO3作氧化剂,铜作还原剂,3mol Cu还原2mol的HNO3 |
Q、W、X、Y、Z是原子序数依次增大的短周期元素,X、Y是金属元素,X的焰色呈黄色.五种元素核电荷数之和为54,最外层电子数之和为20.W、Z最外层电子数相同,Z的核电荷数是W的2倍.工业上一般通过电解氧化物的方法获得Y的单质.则下列说法不正确的是( )
| A、原子半径:X>Y>Q>W |
| B、元素Y与元素Z的最高正化合价之和的数值等于8 |
| C、Q和Z所形成的化合物为共价化合物 |
| D、X、Q和W三种元素形成的化合物的水溶液呈碱性 |
已知次氯酸是比碳酸还弱的酸,反应Cl2+H2O?HCl+HClO达平衡后,要使HClO浓度增大,可加入( )
| A、HCl |
| B、少量Na2SO3 |
| C、少量NaOH |
| D、CaCO3 |
 .试回答:
.试回答: 工业上一般以CO和H2为原料合成甲醇,该反应的热化学方程式为:
工业上一般以CO和H2为原料合成甲醇,该反应的热化学方程式为: