题目内容
18.下表是元素周期表的一部分,请针对表中所列标号为①~⑩的元素回答下列问题.| 族 周期 | IA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
| 二 | ① | ② | ③ | ④ | ||||
| 三 | ⑤ | ⑥ | ⑦ | ⑧ | ⑨ | ⑩ |
(2)第三周期元素除⑩外原子半径最小的是Cl(填元素符号),这些元素的最高价氧化物对应水化物中碱性最强的是NaOH(填化学式,下同),具有两性的是Al(OH)3.
分析 由元素在周期表中的位置可知,①为C,②为N,③为O,④为F,⑤为Na,⑥为Mg,⑦为Al,⑧为S,⑨为Cl,⑩为Ar,然后利用元素及其单质、化合物的性质来解答.
解答 解:由元素在周期表中的位置可知,①为C,②为N,③为O,④为F,⑤为Na,⑥为Mg,⑦为Al,⑧为S,⑨为Cl,⑩为Ar,
(1)以上元素中第二周期中F的非金属性最强,在第ⅦA中F的非金属性最强,则F的非金属性最强,碳元素形成的有机物种类最多,
故答案为:F;C;
(2)同周期,从左向右原子半径在减小,则Cl的原子半径在第三周期最小,以上元素中Na的金属性最强,则最高价氧化物对应水化物NaOH的碱性最强,Al元素的最高价氧化物对应水化物Al(OH)3的具有两性,
故答案为:Cl;NaOH;Al(OH)3.
点评 本题考查元素周期表和元素周期律,熟悉元素在元素周期表中的位置是解答本题的关键,并利用元素及其单质、化合物的性质来解答即可,难度不大.

练习册系列答案
相关题目
8.下列说法正确的是( )
| A. | 乙烯的结构简式为CH2CH2 | |
| B. | 烷烃的通式为CnH2n+2,随n值增大,碳元素的质量百分含量逐渐减小 | |
| C. | 1 mol-CH3 含有9 mol 电子 | |
| D. | 己烷有4种同分异构体,它们的熔点、沸点各不相同 |
6.化学与生活、社会密切相关,下列说法不正确的是( )
| A. | 日用品中的塑料、橡胶、糖类等都是有机物 | |
| B. | 生活中经常使用的保鲜膜主要成分是聚乙烯 | |
| C. | 氨很容易液化,液氨气化吸收大量的热,所以液氨常用作制冷剂 | |
| D. | SO2可以用来漂白纸浆、毛、丝、草帽辫、增白食品等 |
13.下列各组物质的无色溶液,不用其它试剂即可鉴别的是( )
①KCl Na2CO3 HCl ②NaHCO3 Ba(OH)2 H2SO4
③HCl NaAlO2 NaHSO4 ④Ca(OH)2 Na2CO3 BaCl2.
①KCl Na2CO3 HCl ②NaHCO3 Ba(OH)2 H2SO4
③HCl NaAlO2 NaHSO4 ④Ca(OH)2 Na2CO3 BaCl2.
| A. | ①② | B. | ②③ | C. | ①③④ | D. | ①②④ |
3.我国积极启动“蓝天工程”和“绿水工程”,是为了保护生态环境、提高全体人民生活质量的重要举措.下列措施不利于以上工程实施的是( )
| A. | 推广使用燃煤脱硫技术,防治SO2污染 | |
| B. | 减少重金属、农药和难分解有机物的排放 | |
| C. | 加大石油、煤炭的开采速度,增加化石燃料的供应量 | |
| D. | 开发新能源和新致冷剂,减少CO2和氟氯烃等物质的大量排放 |
10.下列溶液中,可以大量共存的离子组是( )
| A. | H+、Na+、SO42-、HCO3- | B. | NH4+、Fe3+、SO42-、OH- | ||
| C. | Na+、K+、AlO2-、Cl- | D. | Fe2+、Ba+、SO42-、NO3- |
7.近年来,违章违法开采的煤矿经常发生瓦斯爆炸的事故,当瓦斯中甲烷和氧气的质量比为1:4时,极易发生爆炸,此时甲烷和氧气的体积比是( )
| A. | 1:1 | B. | 1:2 | C. | 1:4 | D. | 2:1 |
8.下列关于甲烷的说法中,不正确的是( )
| A. | 是天然气的主要成分 | B. | 甲烷是正四面体型分子 | ||
| C. | 分子中C的质量分数为75% | D. | 甲烷不能发生氧化反应 |
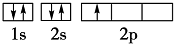 ,核外有5种运动状态不同的电子.
,核外有5种运动状态不同的电子.