题目内容
已知N2(g)+3H2(g)==2NH3(g) △H=-92 kJ·mol-1。且1 mol N≡N键完全断裂时吸收热量946 kJ, 1 mol H-N键形成时放出热量391 kJ,则氢气中1mol H-H键断裂时吸收热量为( )
| A.920 kJ | B.557 kJ | C.436 kJ | D.188 kJ |
C
在化学反应中,断键吸收和能量和形成化学键所放出的能量的差值就是反应热,所以有946 kJ/mol+3X-2×3×391 kJ/mol=-92 kJ/mol,解得X=436 kJ/mol.所以答案选C。

练习册系列答案
相关题目
 CH3OH(g) ΔH1
CH3OH(g) ΔH1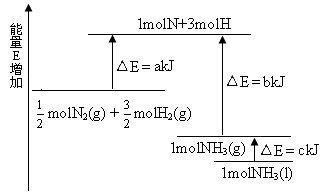
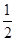 N2(g)+
N2(g)+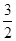 H2(g) ===NH3(1)△H=(b+c-a)kJ·mol-1
H2(g) ===NH3(1)△H=(b+c-a)kJ·mol-1 CH3OH(g); ΔH1
CH3OH(g); ΔH1
 ══
══

 ══
══

 ══2CO2(g)+2H2O(l)
══2CO2(g)+2H2O(l)
 ══
══
