题目内容
(14分)工业上用铝土矿(主要成分为Al2O3,Fe2O3等)提取Al2O3作冶炼铝的原料,由熔盐电解法获得的粗铝中含一定量的金属钠和氢气,这些杂质可采用吹气精炼法除去,产生的尾气经处理后可用于钢材镀铝。工艺流程如下图所示:
(已知:NaCl熔点为801℃;AlCl3在181℃升华)
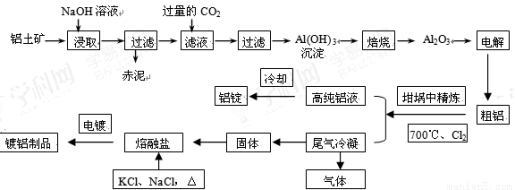
(1)赤泥中的主要成分是 (化学式);向滤液中通入过量CO2所发生反应的离子方程式为 。
(2)精炼前,需清除坩埚表面的氧化铁和石英砂,防止精炼时它们分别与铝发生置换反应产生新的杂质,则铝和氧化铁反应的化学方程式为 。
(3)将Cl2连续通入坩埚中的粗铝熔体,杂质随气泡上浮而除去。气泡的主要成分除Cl2外还含有______。固态杂质粘附于气泡上,在熔体表面形成浮渣,浮渣中肯定存在________。
(4)镀铝电解池中,金属铝为阳极,熔融盐电镀液中铝元素主要以AlCl4-形式存在,则阳极的电极反应式为_____________。
(5)钢材镀铝后,抗腐蚀性能会大大增强,其原因是_____________。
(1)Fe2O3 ; AlO2—+2H2O+CO2=Al(OH)3↓+HCO3—
(2)Fe2O3+2Al  Al2O3+2Fe;(3)HCl和AlCl3;NaCl ;(4)Al-3e-+4Cl-= AlCl4-
Al2O3+2Fe;(3)HCl和AlCl3;NaCl ;(4)Al-3e-+4Cl-= AlCl4-
(5)表面形成的致密氧化铝膜能防止钢材腐蚀或致密的氧化铝膜将环境中的电解质溶液与内层金属隔离
【解析】
试题分析:(1)铝土矿的主要成分为Al2O3,Fe2O3,当向其中加入NaOH溶液时Al2O3发生反应Al2O3+2NaOH=2NaAlO2+2H2O;产生可溶性的物质,而Fe2O3不能在水中溶解,沉在容器的底部,成为阳极泥。所以赤泥中的主要成分是Fe2O3;向滤液中通入过量CO2所发生反应的离子方程式是AlO2—+2H2O+CO2=Al(OH)3↓+HCO3—;(2)铝和氧化铁在高温下发生铝热反应,反应的化学方程式为Fe2O3+2Al  Al2O3+2Fe;(3)将Cl2连续通入坩埚中的粗铝熔体,杂质随气泡上浮而除去。当通入氯气时,气泡的主要成分除Cl2外还含有Al与Cl2反应产生的AlCl3及表面水分反应产生的HCl。固态杂质粘附于气泡上,在熔体表面形成浮渣,由于Al2O3是从NaOH溶液中过滤出来的,表面有NaOH杂质,当通入Cl2是发生反应产生NaCl,所以浮渣中肯定存在NaCl。(4)镀铝电解池中,金属铝为阳极,熔融盐电镀液中铝元素主要以AlCl4-形式存在,则阳极发生氧化反应,该电极的电极反应式为Al-3e-+4Cl-= AlCl4-;(5)钢材镀铝后,抗腐蚀性能会大大增强,其原因是表面形成的致密氧化铝膜能防止钢材腐蚀或致密的氧化铝膜将环境中的电解质溶液与内层金属隔离。
Al2O3+2Fe;(3)将Cl2连续通入坩埚中的粗铝熔体,杂质随气泡上浮而除去。当通入氯气时,气泡的主要成分除Cl2外还含有Al与Cl2反应产生的AlCl3及表面水分反应产生的HCl。固态杂质粘附于气泡上,在熔体表面形成浮渣,由于Al2O3是从NaOH溶液中过滤出来的,表面有NaOH杂质,当通入Cl2是发生反应产生NaCl,所以浮渣中肯定存在NaCl。(4)镀铝电解池中,金属铝为阳极,熔融盐电镀液中铝元素主要以AlCl4-形式存在,则阳极发生氧化反应,该电极的电极反应式为Al-3e-+4Cl-= AlCl4-;(5)钢材镀铝后,抗腐蚀性能会大大增强,其原因是表面形成的致密氧化铝膜能防止钢材腐蚀或致密的氧化铝膜将环境中的电解质溶液与内层金属隔离。
考点:考查电解反应原理的应用、铝热反应、铝元素的电子及化合物的性质、金属的腐蚀与保护的知识。

(10分)蛇纹石可用于生产氢氧化镁,简要工程如下:
Ⅰ.制取粗硫酸镁:用酸液浸泡蛇纹石矿粉,过滤,并在常温常压下结晶,制得粗硫酸镁(其中常含有少量Fe3+、Al3+、Fe2+等杂质离子)
Ⅱ.提纯粗硫酸镁,将粗硫酸镁在酸性条件下溶解,加入适量的0.1mol/LH2O2溶液,再调节溶液pH至7~8,并分离提纯。
Ⅲ.制取氢氧化镁,向步骤II所得溶液中加入过量氨水。
已知:金属离子氢氧化物沉淀所需pH
Fe3+ | Al3+ | Fe2+ | Mg2+ | |
开始沉淀时 | 1.5 | 3.3 | 6.5 | 9.4 |
沉淀完全时 | 3.7 | 5.2 | 9.7 | 12.4 |
请回答:
(1)步骤II中加入适量的0.1mol/LH2O2溶液的目的是 ;可用于调节溶液pH至7~8的最佳试剂是 (填字母序号)
A.MgO B.Na2CO3 C.蒸馏水 D.NaOH .
(2)工业上常以Mg2+的转化率为考查指标,确定步骤III制备氢氧化镁工艺过程的适宜条件。
其中,反应温度与Mg2+转化率的关系如图所示。
①步骤III中制备氢氧化镁反应的离子方程式为 。根据图中所示50℃前温度与Mg2+转化率之间的关系,可判断此反应是 (填“吸热”或“放热”反应)

②图中,温度升高至50℃以上Mg2+转化率下降的可能原因是 。
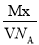 表示的是( )
表示的是( )