题目内容
10.下列表示对应化学反应的离子方程式正确的是( )| A. | 氢氧化亚铁在空气中的变化:4Fe(OH)2+2H2O+O2═4Fe(OH)3 | |
| B. | AlCl3溶液中加入过量的浓氨水:Al3++4NH3•H2O═AlO${\;}_{2}^{-}$+4NH4++2H2O | |
| C. | 向Ca(HCO3)2溶液中滴加过量的NaOH溶液:Ca2++HCO3-+OH-═CaCO3↓+H2O | |
| D. | 用FeCl3溶液腐蚀铜线路板:Cu+Fe3+═Cu2++Fe2+ |
分析 A.氢氧化亚铁不稳定,易被氧气氧化生成氢氧化铁;
B.氢氧化铝属于两性氢氧化物,能和强碱反应但和弱碱不反应;
C.向Ca(HCO3)2溶液中滴加过量的NaOH溶液,二者反应生成碳酸钙、碳酸钠和水;
D.转移电子不守恒、电荷不守恒.
解答 解:A.氢氧化亚铁不稳定,易被氧气氧化生成氢氧化铁,化学方程式4Fe(OH)2+2H2O+O2═4Fe(OH)3为,故A正确;
B.氢氧化铝属于两性氢氧化物,能和强碱反应但和弱碱不反应,离子方程式为Al3++3NH3•H2O=Al(OH)3↓+3NH4+,故B错误;
C.向Ca(HCO3)2溶液中滴加过量的NaOH溶液,二者反应生成碳酸钙、碳酸钠和水,离子方程式为Ca2++2HCO3-+2OH-═CaCO3↓+2H2O+CO32-,故C错误;
D.转移电子不守恒、电荷不守恒,离子方程式为Cu+2Fe3+═Cu2++2Fe2+,故D错误;
故选A.
点评 本题考查离子方程式正误判断,为高频考点,明确物质性质及离子方程式书写规则是解本题关键,涉及氧化还原反应、复分解反应,易错选项是BC.

练习册系列答案
 活力课时同步练习册系列答案
活力课时同步练习册系列答案
相关题目
20.NA为阿伏伽德罗常数的值.下列说法正确的是( )
| A. | 标准状况下,2.24LCl2溶于水时转移的电子数为0.1NA | |
| B. | 过氧化钠与水反应时,生成0.1molO2时转移的电子数为0.2NA | |
| C. | 标准状况下,2.24LNO2与水反应生成NO3-的数目为0.1NA | |
| D. | 用惰性电极电解饱和食盐水,生成4.0gNaOH的同时,生成的气体分子总数为0.05NA |
1.设NA为阿伏加德罗常数的数值,在常温常压下,下列说法正确的是( )
| A. | 18g水所含分子数目为NA,体积约为24.5L | |
| B. | 0.1mol•L-1的NaNO3溶液中含有0.1NA个NO3- | |
| C. | 1mol Fe与足量的盐酸反应,转移3NA个电子 | |
| D. | 2.3g钠离子所含电子数目为1NA |
18.香草醛是一种食品添加剂,可由愈创木酚作原料合成,合成路线如图所示.下列说法正确的是( )


| A. | 在上述三步反应中理论上只有①生成②的反应原子利用率为100% | |
| B. | 氯化铁溶液和碳酸氢钠溶液都能鉴别①④ | |
| C. | ②③分子内含手性碳原子 | |
| D. | 在氢氧化钠溶液中,等物质的量的①和③分别消耗NaOH物质的量之比为1:2 |
19.下列说法正确的是( )
| A. | 平衡膳食就是各食物都要吃 | |
| B. | 摄入食物中的营养素种类齐全,数量充足,比例适当且与人体的需要的保持平衡才是合理的膳食结构 | |
| C. | 淀粉、油脂、蛋白质为人体提供热能,所以只要这三种摄入量足够就可 | |
| D. | 为维持人体内电解质平衡,人在大量出汗后应及时补充Ca2+离子 |

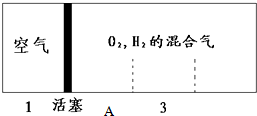 如图所示装置,密闭容器内分别充入空气和H2、O2的混合气体在可移动的活塞两边,在标准状况下若将H2、O2的混合气体点燃引爆,活塞先左弹,恢复原温度后,活塞右滑停留于容器的中央A处,则原来H2、O2的体积比最接近于7:2 或4:5;此比例的H2和O2混合气体的平均摩尔质量为8.67g/mol或18.67g/mol.
如图所示装置,密闭容器内分别充入空气和H2、O2的混合气体在可移动的活塞两边,在标准状况下若将H2、O2的混合气体点燃引爆,活塞先左弹,恢复原温度后,活塞右滑停留于容器的中央A处,则原来H2、O2的体积比最接近于7:2 或4:5;此比例的H2和O2混合气体的平均摩尔质量为8.67g/mol或18.67g/mol.
 +CO2+H2O→NaHCO3+
+CO2+H2O→NaHCO3+ .
.