题目内容
用0.1mol?L-1的氢氧化钠滴定0.10mol?L-1的醋酸,滴定过程中不可能出现的结果是( )
分析:从溶液呈电中性的角度分析该题,溶液中存在c(Na+)+c(H+)=c(OH-)+c(CH3COO-).
解答:解:溶液中存在c(Na+)+c(H+)=c(OH-)+c(CH3COO-),则
A.如c(Na+)>c(CH3COO-),根据溶液呈电中性,则一定有c(OH-)>c(H+),故A正确;
B.如c(CH3COO-)>c(Na+),根据溶液呈电中性,则一定有c(OH-)<c(H+),故B错误;
C.如c(Na+)=c(CH3COO-),根据溶液呈电中性,则一定有c(OH-)=c(H+),故C正确;
D.如c(CH3COO-)>c(Na+),根据溶液呈电中性,则一定有c(H+)>c(OH-),故D正确.
故选C.
A.如c(Na+)>c(CH3COO-),根据溶液呈电中性,则一定有c(OH-)>c(H+),故A正确;
B.如c(CH3COO-)>c(Na+),根据溶液呈电中性,则一定有c(OH-)<c(H+),故B错误;
C.如c(Na+)=c(CH3COO-),根据溶液呈电中性,则一定有c(OH-)=c(H+),故C正确;
D.如c(CH3COO-)>c(Na+),根据溶液呈电中性,则一定有c(H+)>c(OH-),故D正确.
故选C.
点评:本题考查溶液离子浓度大小的比较,题目难度不大,解答本题的关键是从溶液电中性的角度思考.

练习册系列答案
相关题目
下列图象表达正确的是( )


| A、图①表示25℃时,用0.1mol?L-1盐酸滴定20mL 0.1mol?L-1氨水 | B、图②表示常温下,等量锌粉分别与两份足量的等体积等浓度的盐酸反应 | C、图③表示向CaCl2和盐酸的混合溶液中滴加Na2CO3溶液 | D、图④表示向醋酸溶液中滴入氨水 |
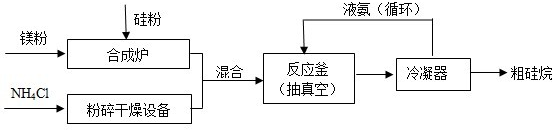
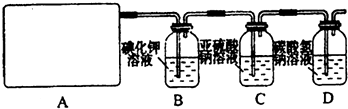
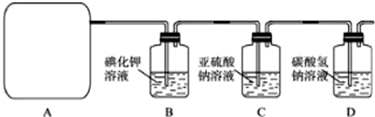
 (2013?海淀区二模)氮化硅膜与二氧化硅膜相比较具有表面化学性能稳定等优点,故氮化硅膜可用于半导体工业.为生成氮化硅膜,可以用NH3和SiH4(硅烷)在一定条件下反应并在600℃的加热基板上生成氮化硅膜:
(2013?海淀区二模)氮化硅膜与二氧化硅膜相比较具有表面化学性能稳定等优点,故氮化硅膜可用于半导体工业.为生成氮化硅膜,可以用NH3和SiH4(硅烷)在一定条件下反应并在600℃的加热基板上生成氮化硅膜: