题目内容
将n mol Al2O3和Fe2O3的混合物溶于100 mL盐酸中,然后逐滴加入1 mol·L-1的氢氯化钠溶液,其结果如下图所示: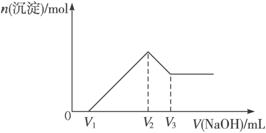
若保持混合物总物质的量不变,Al2O3与Fe2O3按不同比例混合进行上述实验(其他条件不变),当![]() 变大时,关于V1、V2、V3的变化的判断正确的是( )
变大时,关于V1、V2、V3的变化的判断正确的是( )
A.V1变大 B.V2不变 C.V3变小 D.(V3-V1)不变
B
解析:盐酸过量,Al2O3和Fe2O3总物质的量不变,V1不变,A项错误;V2不变,B项正确;V3变大,C项错误;(V3-V1)变大,D项错误。

练习册系列答案
 龙人图书快乐假期暑假作业郑州大学出版社系列答案
龙人图书快乐假期暑假作业郑州大学出版社系列答案
相关题目
今用铝、稀硫酸和氢氧化钠为原料,在实验室制备一定量的氢氧化铝,可以分别采用如下化学方程式所表示的两种方法:
①2Al+3H2SO4====Al2(SO4)3+3H2↑
Al2(SO4)3+6NaOH====2Al(OH)3↓+3Na2SO4
②2Al+2NaOH+2H2O====2NaAlO2+3H2↑
2NaAlO2+H2SO4+2H2O====2Al(OH)3↓+Na2SO4
(1)请将每制取2 mol Al(OH)3所耗费的酸、碱用量记录于下表中,然后说明哪一种方法比较节约试剂。
途 径 | 生成2 mol Al(OH)3所消耗酸碱的物质的量 | |
| n(H2SO4)/mol | n(NaOH)/mol |
①Al→Al3+→Al(OH)2 ②Al→ |
|
|
(2)原料相同,请设计一种更节约试剂,且操作更为简单的方法,(提示:从反应终点是否易于控制角度考虑)。用化学方程式表示并予以说明。
