��Ŀ����
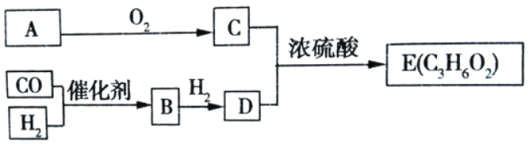
����Ŀ����A�ڱ�״���µ��ܶ�Ϊ1.25gL��1����A��ˮú��(CO��H2)Ϊԭ����һ������ �¿ɻ���л���B��C��D��E�����ת����ϵ��ͼ����֪B��CO��H2�����ʵ���֮��Ϊ 1:1 ��Ӧ�IJ��EΪ��Ũ����ζ����������ˮ����״Һ�塣
��ش�
(1)�л���C�ֺ��еĹ�����������_____��
(2)C+D��E�ķ�Ӧ������_____��
(3)�л���B��һ��������ת��ΪD�Ļ�ѧ����ʽ��_____��
(4)����˵������ȷ����_____��
A���л���D������Ʒ�Ӧ��ˮ������Ʒ�ӦҪ����
B���л���C��D��E���ñ���̼������Һ����
C��ʵ�����Ʊ�Eʱ��Ũ������Ҫ����������
D���л��� B��C���ܱ����Ƽ���������ͭ����Һ������KMnO4��Һ����
���𰸡��Ȼ� ������Ӧ(��ȡ����Ӧ) HCHO+H2![]() CH3OH ACD
CH3OH ACD
��������
A���ܶ�Ϊ1.25gL-1������Է�������Ϊ1.25��22.4=28��ӦΪCH2=CH2��B �� CO �� H2�����ʵ���֮��Ϊ 1��1 ��Ӧ�IJ����BΪHCHO�����������ɵ�DΪCH3OH��E Ϊ��Ũ����ζ����������ˮ����״Һ�壬ӦΪ���࣬�ɷ���ʽ��֪ӦΪCH3COOCH3����CΪCH3COOH���Դ˽����⡣
(1)CΪCH3COOH�����еĹ�����Ϊ�Ȼ���
(2)C��D����������Ӧ����E��ҲΪȡ����Ӧ��
(3)�л��� B ��һ��������ת��Ϊ D �Ļ�ѧ����ʽ��HCHO+H2![]() CH3OH��
CH3OH��
(4)A��DΪ�״������ϵ��ǻ��ⲻ��ˮ�е�����ã���������Ʒ�Ӧ����ˮ������Ʒ�Ӧ���ң���A����
B���л����������̼���Ʒ�Ӧ�������壬������ڱ���̼������Һ���ɿ��ñ���̼������Һ���𣬹�B��ȷ��
C��ʵ�����Ʊ��������ʱ��Ũ������Ҫ������ã�������ˮ���ã���C����
D��������������ͭ��������ز�����������Ӧ����D����
�ʴ�Ϊ��ACD��

 ����ѧҵ���Ե�����ϵ�д�
����ѧҵ���Ե�����ϵ�д�����Ŀ�������£��й����ʵ��ܶȻ����±���ʾ��
���� | CaCO3 | MgCO3 | Ca(OH)2 | Mg(OH)2 | Fe(OH)3 |
Ksp | 4.96��10��9 | 6.82��10��6 | 4.68��10��6 | 5.61��10��12 | 2.64��10��39 |
�����й�˵������ȷ���ǣ� ��
A.�����£���ȥNaCl��Һ�е�MgCl2���ʣ�ѡ��NaOH��Һ��Na2CO3��ҺЧ����
B.�����£���ȥNaCl��Һ�е�CaCl2���ʣ�ѡ��Na2CO3��Һ��NaOH��ҺЧ����
C.�����£�����Mg2����Fe3������Һ�еμ�NaOH��Һ�������ֳ�����������Һ��pH��8ʱ��c(Mg2��)��c(Fe3��)��2.125��1021��1
D.������Ca(OH)2�Ʊ�NaOH