题目内容
【题目】根据下列实验现象,所得结论错误的是( )
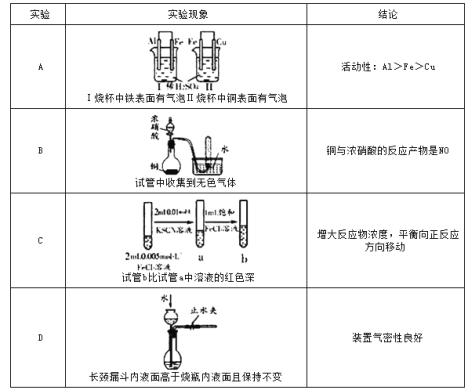
A.AB.BC.CD.D
【答案】B
【解析】
![]() 根据原电池的工作原理,左烧杯中铁表面有气泡,说明负极为铝,正极为铁,金属活动性
根据原电池的工作原理,左烧杯中铁表面有气泡,说明负极为铝,正极为铁,金属活动性![]() ,右边烧杯中铜表面有气泡,说明铁为负极,铜为正极,金属活动性
,右边烧杯中铜表面有气泡,说明铁为负极,铜为正极,金属活动性![]() ,则活动性为
,则活动性为![]() ,故A正确;
,故A正确;
B.Cu与浓硝酸反应,反应中的化合价变化为:![]() 中N元素由
中N元素由![]() 价降低为
价降低为![]() 中N元素
中N元素![]() 价,
价,![]() 是氧化剂,
是氧化剂,![]() 是还原产物,方程式为:
是还原产物,方程式为:![]() ;生成的红棕色二氧化氮和水发生氧化还原反应,
;生成的红棕色二氧化氮和水发生氧化还原反应,![]() ,所以图中试管中收集到无色气体为一氧化氮,但不是铜和浓硝酸反应生成一氧化氮,故B错误;
,所以图中试管中收集到无色气体为一氧化氮,但不是铜和浓硝酸反应生成一氧化氮,故B错误;
C.![]() 遇
遇![]() 发生反应
发生反应![]() ,
,![]() 为血红色,增大氯化铁溶液的浓度,根据溶液颜色变化来判断反应方向,如果溶液颜色加深,则说明平衡向正反应方向移动,所以能达到实验目的,故C正确;
为血红色,增大氯化铁溶液的浓度,根据溶液颜色变化来判断反应方向,如果溶液颜色加深,则说明平衡向正反应方向移动,所以能达到实验目的,故C正确;
D.该装置的气密性检查,主要是通过气体压强增大看体积变化来进行检验,夹紧止水夹,向长颈漏斗中加水至其液面高于烧瓶内的液面,一段时间后,看液面高度差有无变化,变化说明装置漏气,反之不漏气,故D正确;
故选 B.

 时刻准备着暑假作业原子能出版社系列答案
时刻准备着暑假作业原子能出版社系列答案 暑假衔接教材期末暑假预习武汉出版社系列答案
暑假衔接教材期末暑假预习武汉出版社系列答案 假期作业暑假成长乐园新疆青少年出版社系列答案
假期作业暑假成长乐园新疆青少年出版社系列答案【题目】在相同温度和体积下,对反应![]()
![]()
![]() 进行甲、乙、丙、丁四组实验,实验起始时放入容器内各组分的物质的量见下表
进行甲、乙、丙、丁四组实验,实验起始时放入容器内各组分的物质的量见下表
物质的量 |
|
|
|
|
甲 | amol | amol | 0mol | 0mol |
乙 | 2amol | amol | 0mol | 0mol |
丙 | 0mol | 0mol | amol | amol |
丁 | amol | 0mol | amol | amol |
上述四种情况达到平衡后,![]() 最大的是
最大的是![]()
A.甲B.乙C.丙D.丁
【题目】硝酸是一种重要的化工原料。以![]() 和
和![]() 为原料合成氨气
为原料合成氨气![]() 。取一定量的
。取一定量的![]() 和
和![]() 置于密闭容器中进行反应。已知化学平衡常数K与温度的关系如表:
置于密闭容器中进行反应。已知化学平衡常数K与温度的关系如表:
| 200 | 300 | 400 |
K |
|
|
|
(1)写出该反应的平衡常数表达式______。
(2)K1和![]() 比较:
比较:![]() ______
______![]() 填写“
填写“![]() ”、“
”、“![]() ”或“
”或“![]() ”
”![]()
(3)在![]() 时该反应进行一段时间后,测定
时该反应进行一段时间后,测定![]() 、
、![]() 和
和 ![]() 的物质的量分别为2mol、1mol和2mol,则此时反应速率
的物质的量分别为2mol、1mol和2mol,则此时反应速率![]() ______
______![]() 。
。 ![]() 填写“
填写“![]() ”、“
”、“![]() ”、“
”、“![]() ”或“不能确定”
”或“不能确定”![]()