题目内容
在加热情况下,用足量CO还原7 g铁的氧化物组成的混合物,产生气体全部通入足量石灰水中得到12.5 g沉淀,此混合物不可能为:
- A.FeO、Fe2O3
- B.FeO、Fe3O4
- C.Fe2O3、Fe3O4
- D.FeO、Fe2O3、Fe3O4
B
试题分析:生成的气体是CO2,所以得到的沉淀是碳酸钙,物质的量是0.125mol,则关键原子守恒可知,氧化物中氧元素的质量是0.125mol×16g/mol=2g,则铁元素的质量是7g-2g=5g,所以氧化物中铁原子和氧原子的原子个数之比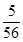 ︰
︰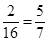 ,即该化合物的平均组成是Fe5O7。A中FeO、Fe2O3 的物质的量满足1︰2即可;C中Fe2O3、Fe3O4的物质的量满足1︰1即可;D中FeO、Fe2O3、Fe3O4的物质的量满足1︰3︰1即可,所以答案选B。
,即该化合物的平均组成是Fe5O7。A中FeO、Fe2O3 的物质的量满足1︰2即可;C中Fe2O3、Fe3O4的物质的量满足1︰1即可;D中FeO、Fe2O3、Fe3O4的物质的量满足1︰3︰1即可,所以答案选B。
考点:考查铁的氧化物组成的有关计算和判断
点评:该题是难度较大的计算题,对学生的综合能力要求高。该题的难点不在于计算氧化物的平均组成,而在于通过平均组成进行的讨论和排除。本题学生不易得分。
试题分析:生成的气体是CO2,所以得到的沉淀是碳酸钙,物质的量是0.125mol,则关键原子守恒可知,氧化物中氧元素的质量是0.125mol×16g/mol=2g,则铁元素的质量是7g-2g=5g,所以氧化物中铁原子和氧原子的原子个数之比
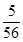 ︰
︰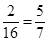 ,即该化合物的平均组成是Fe5O7。A中FeO、Fe2O3 的物质的量满足1︰2即可;C中Fe2O3、Fe3O4的物质的量满足1︰1即可;D中FeO、Fe2O3、Fe3O4的物质的量满足1︰3︰1即可,所以答案选B。
,即该化合物的平均组成是Fe5O7。A中FeO、Fe2O3 的物质的量满足1︰2即可;C中Fe2O3、Fe3O4的物质的量满足1︰1即可;D中FeO、Fe2O3、Fe3O4的物质的量满足1︰3︰1即可,所以答案选B。考点:考查铁的氧化物组成的有关计算和判断
点评:该题是难度较大的计算题,对学生的综合能力要求高。该题的难点不在于计算氧化物的平均组成,而在于通过平均组成进行的讨论和排除。本题学生不易得分。

练习册系列答案
 教学练新同步练习系列答案
教学练新同步练习系列答案
相关题目