题目内容
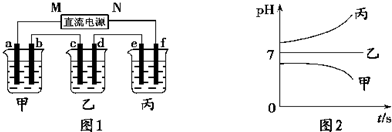
有A、B、C三种电解质溶液分别装在三个烧杯中,插有石墨电极,并按下图所示方式在电路中连接。闭合开关K后,测得各支路电流强度I1≈IⅡ(其中IⅡ 略小)。若撤去B,测知电流强度IA《Ic;若撒去C,并将A、B两溶液混匀后均分为 两等份,再重置于电路I、Ⅱ处,测知通过A、B混合溶液的电流强度与先前通过A 溶液的电流强度的相对大小关系为:1AB》IA。已知A、B、C分别选自下列溶液:0.1mol·L-1盐酸、0.1mol·L-1醋酸、0.1mol·L-1NaCl 溶液、0.1mol·L-1硫酸、0.1mol·L-1NaOH溶液、 0.1mol·L-1氨水,且25℃时A溶液PH<7。

(1)指出A、B、C是(或可能是)什么溶液?A________; B________;C________。
(2)若向C溶液中滴入酚酞试剂呈红色,则C是________;将A、B、C分别以等体 积进行两两混合,结果是哪种组合的混合液中,水的电离度最大?(填“A”“B”或“C”)。
答案:
解析:
解析:
(1)0.1mol.L-1醋酸 0.1 mol.L-1氨水 盐酸(或NaCl、H2SO4、NaOH)(2)NaOH溶液 AB
|

练习册系列答案
 津桥教育计算小状元系列答案
津桥教育计算小状元系列答案
相关题目