题目内容
14.(1)将下列离子Na+、Ag+、Cu2+、H+、NO3-、Cl-、CO32-、OH-按可能大量共存于同一溶液的情况,把他们分成A、B两组.A组显酸性,除H+外还有NO3-、Ag+、Cu2+离子
B组显碱性,除OH-外还有CO32-、Cl-、Na+离子
(2)实验室制备氢氧化铁胶体的化学方程式为FeCl3+3H2O$\frac{\underline{\;\;△\;\;}}{\;}$Fe(OH)3(胶体)+3HCl.
分析 (1)H+能分别与CO32-、OH-反应,则B组一定含有CO32-、OH-,且CO32-、OH-均与Ag+、Cu2+、H+反应,则A中一定含有Ag+、Cu2+、H+,又Ag+、Cl-反应,所以Cl-在B中,然后结合电荷守恒分析A、B中的离子;
(2)氯化铁在沸水中水解生成胶体.
解答 解:(1)H+能分别与CO32-、OH-反应,则B组一定含有CO32-、OH-,且CO32-、OH-均与Ag+、Cu2+、H+反应,则A中一定含有Ag+、Cu2+、H+,又Ag+、Cl-反应,所以Cl-在B中,又溶液不显电性,由电荷守恒可知,A组一定存在的阴离子为NO3-,
即A组含有的离子为NO3-、Ag+、Cu2+、H+,B组含有的离子为CO32-、OH-、Cl-、Na+,
故答案为:NO3-;Ag+;Cu2+;CO32-;Cl-;Na+;
(2)实验室制备氢氧化铁胶体的方法是:加热烧杯中的水至沸腾,向沸水滴加几滴饱和氯化铁溶液,继续煮沸至溶液呈红褐色,即停止加热,要注意实验过程不能用玻璃棒搅拌,否则溶液出现浑浊;当反应体系呈现红褐色,即制得氢氧化铁胶体,应立即停止加热,否则也容易出现浑浊,产生红褐色的氢氧化铁沉淀,往沸水中滴加饱和氯化铁溶液后,可稍微加热煮沸,但不宜长时间加热,反应原理为:FeCl3+3H2O$\frac{\underline{\;\;△\;\;}}{\;}$Fe(OH)3(胶体)+3HCl,
故答案为:FeCl3+3H2O$\frac{\underline{\;\;△\;\;}}{\;}$Fe(OH)3(胶体)+3HCl.
点评 本题考查离子的共存,为高频考点,把握习题中的信息及常见离子之间的反应为解答的关键,侧重复分解反应的离子共存考查,题目难度不大.

练习册系列答案
相关题目
4.酒类是日常生活中常见的饮品.适量饮酒有利于身体健康,过量酗酒对身体危害极大.下列酒类中,一般认为酒精度最高的是( )
| A. | 啤酒 | B. | 葡萄酒 | C. | 白酒 | D. | 黄酒 |
2.工业上用的铝上矿(主要成分是氧化铝.含氧化铁杂质)为原料冶炼铝的工艺流程如下:
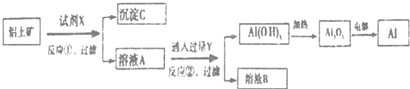
下列叙述正确的是( )

下列叙述正确的是( )
| A. | 反应①中试剂X是氢氧化钠溶液 | |
| B. | 试剂Y是HCI,它与AlO2-反应生成氢氧化铝 | |
| C. | 图中所示转化反应中包含2个氧化还原反应 | |
| D. | 将X与Y试剂进行对换,最终可以达到相同结果 |
9.如表为元素周期表的一部分,请回答有关问题:
(1)元素⑤的名称是硅,表中最活泼的金属是K(填写元素符号).
(2)表中能形成两性氧化物的元素是Al(填写元素符号),请写出该元素的氢氧化物与⑨的最高价氧化物对应水化物反应的化学方程式:Al(OH)3+KOH=KAlO2+2H2O
(3)元素⑥氢化物的化学式为H2S,其稳定性比H2O弱(填“强”或“弱”).
| ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 | |
| 2 | ① | ② | ||||||
| 3 | ③ | ④ | ⑤ | ⑥ | ⑦ | ⑧ | ||
| 4 | ⑨ | ⑩ |
(2)表中能形成两性氧化物的元素是Al(填写元素符号),请写出该元素的氢氧化物与⑨的最高价氧化物对应水化物反应的化学方程式:Al(OH)3+KOH=KAlO2+2H2O
(3)元素⑥氢化物的化学式为H2S,其稳定性比H2O弱(填“强”或“弱”).
6. 对于反应 A(g)+B(g)═C(g)+2D(g)△H>0,达到了平衡状态,在t0时刻改变某条件,反应速率随着时间的变化情况如图所示,这此条件为( )
对于反应 A(g)+B(g)═C(g)+2D(g)△H>0,达到了平衡状态,在t0时刻改变某条件,反应速率随着时间的变化情况如图所示,这此条件为( )
 对于反应 A(g)+B(g)═C(g)+2D(g)△H>0,达到了平衡状态,在t0时刻改变某条件,反应速率随着时间的变化情况如图所示,这此条件为( )
对于反应 A(g)+B(g)═C(g)+2D(g)△H>0,达到了平衡状态,在t0时刻改变某条件,反应速率随着时间的变化情况如图所示,这此条件为( )| A. | 升高温度 | B. | 降低温度 | C. | .增大压强 | D. | 减小压强 |
3.为除去括号内杂质,下列有关试剂和操作办法正确的是( )
| A. | CO2(HCl):饱和碳酸钠溶液,洗气 | B. | 溴苯(溴):稀NaOH溶液,分液 | ||
| C. | 乙烷(乙烯):酸性KMnO4溶液,洗气 | D. | 乙醇(乙酸):KOH溶液,分液 |
 图为某学生进行粗盐提纯实验中过滤操作的示意图,试回答:
图为某学生进行粗盐提纯实验中过滤操作的示意图,试回答: