题目内容
一定条件下,体积为10L的密闭容器中,2molX和1molY进行反应:
2X(g)+Y(g)  Z(g),经60s达到平衡,生成0.3molZ。下列说法正确的是( )
Z(g),经60s达到平衡,生成0.3molZ。下列说法正确的是( )
A.以X浓度变化表示的反应速率为0.01mol/(L•S)
B.将容器体积变为20L,Z的平衡浓度变为原来的1/2
C.若压强增大1倍,则物质Y的转化率增大1倍
D.若降低温度,X的浓度增大,则该反应的△H>0
【答案】
D
【解析】生成0.3molZ,则消耗X是0.3mol,所以X的反应速率是 ,A不正确。增大容器的容积,则压强降低,平衡向逆反应方向移动,Z的平衡浓度小于原来的1/2,B不正确。压强增大1倍,平衡向正反应方向移动,但Y的转化率不一定增大1倍,C不正确。 降低温度,X的浓度增大,说明平衡向逆反应方向移动,因此正反应是吸热反应,D正确,答案选D。
,A不正确。增大容器的容积,则压强降低,平衡向逆反应方向移动,Z的平衡浓度小于原来的1/2,B不正确。压强增大1倍,平衡向正反应方向移动,但Y的转化率不一定增大1倍,C不正确。 降低温度,X的浓度增大,说明平衡向逆反应方向移动,因此正反应是吸热反应,D正确,答案选D。

练习册系列答案
相关题目
工业上制备合成气的工艺主要是水蒸气重整甲烷:CH4(g)+H2O(g) CO(g)+3H2(g);△H=+206 kJ/mol,一定条件下向体积为1 L的密闭容器中充入1 mol CH4和1 mol H2O,测得CH4(g)和CO(g)的浓度随时间变化曲线如图所示,下列说法正确的是 ( )
CO(g)+3H2(g);△H=+206 kJ/mol,一定条件下向体积为1 L的密闭容器中充入1 mol CH4和1 mol H2O,测得CH4(g)和CO(g)的浓度随时间变化曲线如图所示,下列说法正确的是 ( )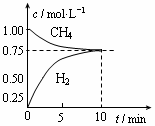
| A.10min时用CH4表示的反应速率为0.075 mol?L-1?min-1 |
| B.使用高效催化剂能够增大CO的产率 |
| C.该条件下反应的平衡常数为0.1875 |
D.升高温度能使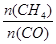 增大 增大 |

 CO(g)+3H2(g);△H=+206 kJ/mol,一定条件下向体积为1 L的密闭容器中充入1 mol CH4和1 mol H2O,测得CH4(g)和CO(g)的浓度随时间变化曲线如图所示,下列说法正确的是 ( )
CO(g)+3H2(g);△H=+206 kJ/mol,一定条件下向体积为1 L的密闭容器中充入1 mol CH4和1 mol H2O,测得CH4(g)和CO(g)的浓度随时间变化曲线如图所示,下列说法正确的是 ( )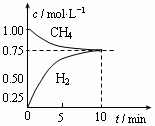
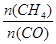 增大
增大