题目内容
1.一定条件下在固定体积的密闭容器中,能表示反应X(g)+2Y(g)?2Z(g)一定达到化学平衡状态的是( )| A. | X、Y、Z的物质的量之比为1:2:2 | |
| B. | X、Y、Z的浓度不再发生变化 | |
| C. | 容器中的压强不再发生变化 | |
| D. | 单位时间内生成n mol Z,同时生成2n mol Y |
分析 根据化学平衡状态的特征解答,当反应达到平衡状态时,正逆反应速率相等,各物质的浓度、百分含量不变,以及由此衍生的一些量也不发生变化,解题时要注意,选择判断的物理量,随着反应的进行发生变化,当该物理量由变化到定值时,说明可逆反应到达平衡状态.
解答 解:A、X、Y、Z的物质的量之比为1:2:2,并不是不变的状态,所以可能是平衡状态,也可能不是平衡状态,故A错误;
B、X、Y、Z的浓度不再发生变化,说明达平衡状态,故B正确;
C、容器中的压强不发生变化,说明气体的物质的量不变,达平衡状态,故C正确;
D、单位时间内生成2n mol Z,同时生成2n mol Y,才达平衡状态,故D错误;
故选BC.
点评 本题考查了化学平衡状态的判断,难度不大,注意当反应达到平衡状态时,正逆反应速率相等,但不为0.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案
相关题目
11.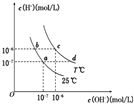 在不同温度下,水溶液中c(H+)与c(OH-)有如图所示关系.下列条件关于离子共存说法中正确的是( )
在不同温度下,水溶液中c(H+)与c(OH-)有如图所示关系.下列条件关于离子共存说法中正确的是( )
 在不同温度下,水溶液中c(H+)与c(OH-)有如图所示关系.下列条件关于离子共存说法中正确的是( )
在不同温度下,水溶液中c(H+)与c(OH-)有如图所示关系.下列条件关于离子共存说法中正确的是( )| A. | a点对应的溶液中大量存在:CO32-、Na+、Cl-、SO42- | |
| B. | b点对应的溶液中大量存在:Fe2+、Ba2+、K+、NO3- | |
| C. | c点对应的溶液中大量存在:Na+、Ba2+、Cl-、Al3+ | |
| D. | d点对应的溶液中大量存在:Na+、K+、ClO-、Cl- |
12.2012年1月16日在阿联酋首都阿布扎比举行的“2012年世界未来能源峰会”上,联合国秘书长潘基文启动联合国“人人享有可持续能源国际年”.下列不能体现“可持续”理念的是( )
| A. | 应用高效洁净的能源转换技术,推广使用节能环保材料 | |
| B. | 大力发展火力发电,解决电力紧张问题 | |
| C. | 研发以高纯硅为核心材料的光伏发电技术 | |
| D. | 大力开发新能源,如核能、太阳能、风能等,减少化石能源的使用 |
9.已知有如下反应:①2BrO3-+Cl2═Br2+2ClO3-,②2FeCl2+Cl2═2FeCl3 ③ClO3-+5Cl-+6H+═3Cl2+3H2O,④2FeCl3+2KI═2FeCl2+2KCl+I2,下列各微粒氧化能力由强到弱的顺序正确的是( )
| A. | ClO3->BrO3->Cl2>Fe3+>I2 | B. | BrO3->Cl 2>ClO3->I2>Fe3+ | ||
| C. | BrO3->ClO3->Cl2>Fe3+>I2 | D. | BrO3->ClO3->Fe3+>Cl2>I2 |
16.如果你家里的食用花生油中不小心混入了水,你将采用的分离方法是( )
| A. | 过滤 | B. | 分液 | C. | 萃取 | D. | 蒸馏 |
6.已知,向Zn2+离子溶液中滴加氨水,生成Zn(OH)2白色沉淀;但是氨水过量时,沉淀又溶解,生成了Zn(NH3)42+.此外,Zn(OH)2既可溶于盐酸,也可溶于过量NaOH溶液中,生成ZnO22-,所以Zn(OH)2是一种两性氢氧化物.
现有4组离子,每组有2种金属离子.可供选用的试剂有:A硫酸B盐酸 C硝酸 D氢氧化钠溶液 E氨水,选择合适试剂可以让一种离子沉淀一种离子保留在溶液中.
试填空:通过合理选择试剂后将两离子分开后保留在溶液中的离子实际存在形式的符号
现有4组离子,每组有2种金属离子.可供选用的试剂有:A硫酸B盐酸 C硝酸 D氢氧化钠溶液 E氨水,选择合适试剂可以让一种离子沉淀一种离子保留在溶液中.
试填空:通过合理选择试剂后将两离子分开后保留在溶液中的离子实际存在形式的符号
| 离子组 | 保留在溶液中的离子 |
| 1Zn2+和Al3+ | |
| 2Zn2+和Mg2+ | |
| 3Zn2+和Ba2+ | |
| 4Fe3+和Al3+ |
13.下列物质露置在空气中,质量会减轻的是( )
| A. | NaOH | B. | Na2O2 | C. | 浓硫酸 | D. | 浓硝酸 |
11.钡和钠相似,也能形成O22-离子的过氧化物,则下列叙述错误的是( )
| A. | 1mol过氧化钠或过氧化钡跟足量水反应都生成0.5mol氧气 | |
| B. | 过氧化钡的化学式是Ba2O2 | |
| C. | 过氧化钡是离子化合物 | |
| D. | 过氧化钠和过氧化钡都是强氧化剂 |