题目内容
如下图所示,常温下U形管内盛有100 mL的溶液,请按要求回答下列问题:
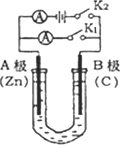
(1)若所盛溶液为CuSO4溶液,打开K2,合并K1,则:A为________极,B极的电极反应式为________.
(2)若所盛溶液为滴有酚酞的NaCl溶液,打开K1,合并K2,则:
①、________极(填A或B)溶液先变红色,原因是________
②、电解池的离子方程式是________
③、反应一段时间后打开K2,若忽略溶液的体积变化和气体的溶解,B极产生气体的体积(折算成标准状况)为11.2 mL,若将溶液充分混合,溶液的pH为________
答案:

练习册系列答案
相关题目


