题目内容
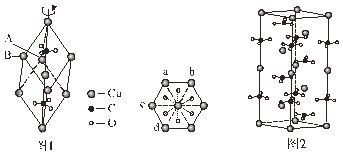
【题目】我国科研人员研究了在 Cu-ZnO-ZrO2 催化剂上CO2加氢制甲醇过程中水的作用机理,其主反应历程如图所示(H2→*H+*H,带*标记的物质是该反应历程中的中间产物或过渡态)。下列说法错误的是
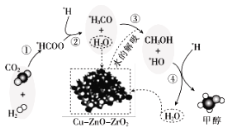
A.第①步中CO2和H2分子中都有化学键断裂
B.水在整个历程中可以循环使用,整个过程不消耗水也不产生水
C.第③步的反应式为:*H3CO+H2O→CH3OH+*HO
D.第④步反应是一个放热过程
【答案】B
【解析】
A. 第①步反应中CO2和H2反应产生*H和*HCOO,可见两种分子中都有化学键断裂,A正确;
B. 根据图示可知:在第③步反应中有水参加反应,第④步反应中有水生成,所以水在整个历程中可以循环使用,整个过程中总反应为CO2+3H2→CH3OH+H2O,整个过程中产生水,B错误;
C. 在反应历程中,第③步中需要水,*H3CO、H2O反应生成CH3OH、*HO,反应方程式为:*H3CO+H2O→CH3OH+*HO,C正确;
D. 第④步反应是*H+*HO=H2O,生成化学键释放能量,可见第④步反应是一个放热过程,D正确;
故答案选B。

【题目】Ⅰ、某化学研究性学习小组为探究元素性质的变化规律,设计了如下实验:
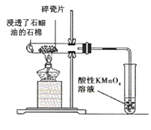
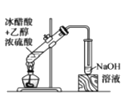
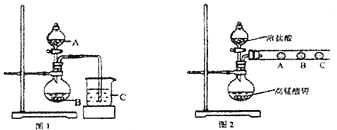
(1)甲同学欲比较N、C、Si的非金属性强弱,设计了图1所示的实验装置,其设计的依据是 ;但该装置存在缺陷,请指出 。
(2)乙同学设计了如图2装置验证元素性质递变规律。A、B、C处分别是蘸有NaBr溶液的棉花、湿润的淀粉KI试纸、湿润的红纸。乙同学可能观察到的现象
A. ;B. ;C. 。
从环保角度考虑,该装置有明显不足,请指出提出改进建议 。
Ⅱ、另一化学研究性学习小组在实验室条件下用以硫酸铜溶液为电解液,用电解的方法实现了粗铜的提纯,并对阳极泥和电解液中金属进行回收和含量测定。已知粗铜中含有少量的锌、铁、银、金等金属和少量矿物杂质(与酸不反应)。
步骤一:电解精制:电解时,粗铜应与电源的 极相连。阴极上的电极反应式为 。
步骤二:电解完成后,该小组同学按以下流程对电解液进行处理:

(1)阳极泥的综合利用:稀硝酸处理阳极泥得到硝酸银稀溶液,请写出该步反应的离子方程式: 。
残渣含有极少量的黄金,如何回收金,他们查阅了有关资料,了解到了一些有关金的信息:
序号 | 反应 | 平衡常数 |
1 |
|
|
2 |
|
|
请根据以上信息简要解释溶解阳极泥不用王水的原因 。
(2)滤液含量的测定:以下是该小组探究滤液的一个实验流程。
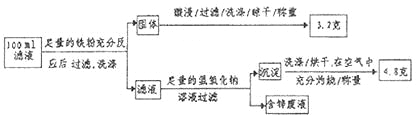
则![]() 滤液中
滤液中![]() 的浓度为
的浓度为 ![]() ,
,![]() 的浓度为
的浓度为 ![]() 。
。