题目内容
发射卫星时可用肼(N2H4)为燃料,用二氧化氮为氧化剂,这两种物质反应生成氮气和水蒸气。已知:N2(g)+2O2(g)![]() 2NO2(g) ΔH1=+67.7 kJ·mol-1 ①
2NO2(g) ΔH1=+67.7 kJ·mol-1 ①
N2H4(g)+O2(g)![]() N2(g)+2H2O(g) ΔH2=-534 kJ·mol-1 ②
N2(g)+2H2O(g) ΔH2=-534 kJ·mol-1 ②
试计算1 mol 肼和二氧化氮完全反应时放出的热量为_________kJ,写出肼与二氧化氮反应的热化学方程式:__________________________________________。
思路解析:由题意可知:
N2(g)+2O2(g)![]() 2NO2(g) ΔH1=+67.7kJ·mol-1 ①
2NO2(g) ΔH1=+67.7kJ·mol-1 ①
N2H4(g)+O2(g)![]() N2(g)+2H2O(g) ΔH2=-534 kJ·mol-1 ②
N2(g)+2H2O(g) ΔH2=-534 kJ·mol-1 ②
根据盖斯定律,为在反应物中消去O2并得到N2H4和NO2的反应。
令②×2-①得:
2 N2H4(g)-N2(g)![]() 2N2(g)+4H2O(g)-2NO2(g);
2N2(g)+4H2O(g)-2NO2(g);
ΔH=2ΔH2-ΔH1,整理得:
2 N2H4(g)+2NO2(g)![]() 3N2(g)+4H2O(g)
3N2(g)+4H2O(g)
ΔH=2ΔH2-ΔH1=534 kJ·mol-1×2-67.7 kJ·mol-1=-1 135.7 kJ·mol-1。
则1 mol N2H4反应放出的热量为567.85 kJ。
答案:567.85
2 N2H4(g)+2NO2(g)![]() 3N2(g)+4H2O(g) ΔH=-1 135.7 kJ·mol-1。
3N2(g)+4H2O(g) ΔH=-1 135.7 kJ·mol-1。

练习册系列答案
 一线名师权威作业本系列答案
一线名师权威作业本系列答案
相关题目
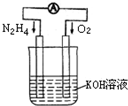 运用化学反应原理研究氮、氧等单质及其化合物的反应有重要意义.
运用化学反应原理研究氮、氧等单质及其化合物的反应有重要意义.