题目内容
(2005·黄冈)已知MgO、 、NaCl和CsCl都是离子晶体,它们的熔沸点由高到低的顺序正确的是
、NaCl和CsCl都是离子晶体,它们的熔沸点由高到低的顺序正确的是
[ ]
A.
B.
C.
D.
答案:B
解析:
解析:
|
思路分析:离子半径 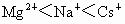 ; ;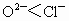 ,且所带电荷 ,且所带电荷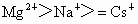 ; ;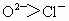 ,所以形成的离子化合物中熔点最高的为MgO,最低的为CsCl,且熔点 ,所以形成的离子化合物中熔点最高的为MgO,最低的为CsCl,且熔点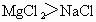 ,故正确顺序为B项. ,故正确顺序为B项.
规律技巧总结:判断离子晶体熔沸点的高低,首先要看构成离子晶体微粒所带电荷的多少与离子半径的大小,所带电荷越多,离子半径越小,离子键越强,晶体的熔沸点也就越高. |

练习册系列答案
相关题目