题目内容
3.由两种气态烃组成的混合气体20mL,跟过量氧气混合后完全燃烧,当燃烧产物通过浓H2SO4,体积减少30mL,然后通过碱石灰,体积又减少40mL(气体均在相同条件下测得),则这两种烃可能为( )| A. | CH4与C2H4 | B. | C2H2与C2H4 | C. | C2H2与C2H6 | D. | CH4与C2H6 |
分析 浓硫酸吸收的是水蒸气,碱石灰吸收的是二氧化碳,设烃的平均组成为CxHy,根据体积之比等于物质的量之比计算平均分子式,然后对各选项进行判断.
解答 解:通过浓硫酸体积减少为烃燃烧生成的水蒸气,通过碱石灰体积减少为烃燃烧生成的二氧化碳,20mL该烃完全燃烧生成二氧化碳40mL、水蒸气30mL,设烃的平均组成为CxHy,则:
根据C原子守恒有:20x=40,解得:x=2,
根据H原子守恒有:20y=30×2,解得:y=3,
则该烃的平均分子式为:C2H3,
根据H原子平均数可知,该烃一定还含有C2H2,根据C原子平均数可知,该烃可能含有C2H6、C2H4,
故该烃可能为C2H4、C2H2或C2H2与C2H6,
故选BC.
点评 本题考查有机物组成的确定、混合物的有关计算,题目难度中等,注意利用平均分子组成判断烃的组成,常用方法有:平均碳法、平均氢法、平均碳氢分子式法、平均式量法.

练习册系列答案
相关题目
13.关于乙烯的化学性质,说法正确的是( )
| A. | 能发生聚合反应 | B. | 能使溴水褪色 | ||
| C. | 可与H2发生加成反应 | D. | 可与HCl加成 |
11.下列说法正确的是( )
| A. | SO2与Na2SO3或NaHCO3溶液能发生反应 | |
| B. | SO2和CO2分别通入BaCl2和Ba(NO3)2溶液中都不产生沉淀 | |
| C. | 浓硫酸具有吸水性,因而能使蔗糖碳化 | |
| D. | SO2和O2混合加热,可生成三氧化硫 |
18. 钠硫电池以熔融金属钠、熔融硫和多硫化钠(Na2Sx)分别作为两个电极的反应物,固体Al2O3陶瓷(可传导Na+)为电解质,其反应原理如图所示.下列说法正确的是( )
钠硫电池以熔融金属钠、熔融硫和多硫化钠(Na2Sx)分别作为两个电极的反应物,固体Al2O3陶瓷(可传导Na+)为电解质,其反应原理如图所示.下列说法正确的是( )
 钠硫电池以熔融金属钠、熔融硫和多硫化钠(Na2Sx)分别作为两个电极的反应物,固体Al2O3陶瓷(可传导Na+)为电解质,其反应原理如图所示.下列说法正确的是( )
钠硫电池以熔融金属钠、熔融硫和多硫化钠(Na2Sx)分别作为两个电极的反应物,固体Al2O3陶瓷(可传导Na+)为电解质,其反应原理如图所示.下列说法正确的是( )| A. | 充电时,电极A接电源的正极 | |
| B. | 充电时,电极B的反应式为Sx2--2e-═xS | |
| C. | 放电时,电极B为负极,Na+由A向B移动 | |
| D. | 放电时,负极反应式为2Na-2e-═2Na+ |
17.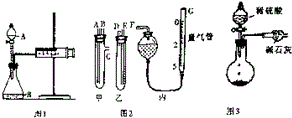 某校化学小组的同学开展测定Na2CO3和NaCl的固体混合物中Na2CO3质量分数的探究实验,他们提出下列实验方案-气体分析法.
某校化学小组的同学开展测定Na2CO3和NaCl的固体混合物中Na2CO3质量分数的探究实验,他们提出下列实验方案-气体分析法.
(1)甲同学用图1所示装置,把Ng的混合物与足量稀硫酸反应后,测定产生的CO2气体的体积,实验开始时检查该装置气密性的方法是关闭A处活塞,将注射器活塞拉出一定距离,一段时间后松开活塞,若活塞能回到原位,证明不漏气,否则漏气.
(2)乙同学用图2代替图1中的发生、收集装置,甲、乙两试管各有两根导管,用橡胶管连接对应接口后,倒置盛有稀硫酸的试管,发生反应,放出气体,则Na2CO3、NaCl的固体混合物和稀硫酸应分别置于甲、乙仪器中(填仪器编号);G管可用化学实验室里的一种常用仪器来代替,你认为这种仪器的名称是碱式滴定管;仪器甲、乙、丙接口的连接方式如下:A连接D,B连接E,C连接F(填写各接口的编号).
(3)丙同学用图3装置测定CO2的质量,该装置存在明显缺陷,从而导致实验误差,请你分析其中使测定结果可能偏大的主要原因CO2气体中混有水蒸气或空气中的CO2和水蒸气进入干燥管中,使测定结果可能偏小的主要原因可能是装置中的CO2没有全部被碱石灰吸收;(上述偏大、偏小的原因各写一条)
(4)某天然碱可看作向CO2和NaOH的反应后的产物所组成,称取天碱样品四份,溶于水后,分别逐滴加入相同浓度的盐酸溶液30毫升,产生CO2的体积(标准状况)如下表:
取3.28g天然碱样品于300℃加热至分解完全(300℃Na2CO3不分解),产生CO2224mL(标准状况)和一定量的水,则该天然碱样品的化学式为Na2CO3•2NaHO3•3H2O.
 某校化学小组的同学开展测定Na2CO3和NaCl的固体混合物中Na2CO3质量分数的探究实验,他们提出下列实验方案-气体分析法.
某校化学小组的同学开展测定Na2CO3和NaCl的固体混合物中Na2CO3质量分数的探究实验,他们提出下列实验方案-气体分析法.(1)甲同学用图1所示装置,把Ng的混合物与足量稀硫酸反应后,测定产生的CO2气体的体积,实验开始时检查该装置气密性的方法是关闭A处活塞,将注射器活塞拉出一定距离,一段时间后松开活塞,若活塞能回到原位,证明不漏气,否则漏气.
(2)乙同学用图2代替图1中的发生、收集装置,甲、乙两试管各有两根导管,用橡胶管连接对应接口后,倒置盛有稀硫酸的试管,发生反应,放出气体,则Na2CO3、NaCl的固体混合物和稀硫酸应分别置于甲、乙仪器中(填仪器编号);G管可用化学实验室里的一种常用仪器来代替,你认为这种仪器的名称是碱式滴定管;仪器甲、乙、丙接口的连接方式如下:A连接D,B连接E,C连接F(填写各接口的编号).
(3)丙同学用图3装置测定CO2的质量,该装置存在明显缺陷,从而导致实验误差,请你分析其中使测定结果可能偏大的主要原因CO2气体中混有水蒸气或空气中的CO2和水蒸气进入干燥管中,使测定结果可能偏小的主要原因可能是装置中的CO2没有全部被碱石灰吸收;(上述偏大、偏小的原因各写一条)
(4)某天然碱可看作向CO2和NaOH的反应后的产物所组成,称取天碱样品四份,溶于水后,分别逐滴加入相同浓度的盐酸溶液30毫升,产生CO2的体积(标准状况)如下表:
| 样品号 | Ⅰ | Ⅱ | Ⅲ | Ⅳ |
| 盐酸溶液的体积/mL | 30 | 30 | 30 | 30 |
| 样品质量/g | 3.32 | 4.15 | 5.81 | 7.47 |
| 二氧化碳的体积/mL | 672 | 840 | 896 | 672 |
18.1919年,科学家第一次实现了人类多年的梦想--人工转变元素.这个核反应如下:${\;}_{7}^{14}$N+${\;}_{2}^{4}$He→${\;}_{8}^{17}$O+${\;}_{1}^{1}$H下列叙述正确的是( )
| A. | ${\;}_{8}^{17}$O原子核内有9个质子 | B. | H原子核内有1个中子 | ||
| C. | O2和O3互为同位素 | D. | 32He和42He是两种不同的核素 |

 .
. .
. .
.