题目内容
 ①图中电解质溶液为硫酸铜溶液,则Fe电极是
①图中电解质溶液为硫酸铜溶液,则Fe电极是负极
负极
(填“正极”或“负极”,下同),其电极反应式为Fe-2e-═Fe2+;
Fe-2e-═Fe2+;
,该反应是氧化
氧化
(填“氧化”或“还原”,下同)反应;Cu电极是正极
正极
,其电极反应式为Cu2++2e-═Cu
Cu2++2e-═Cu
,该反应是还原
还原
反应.②氯碱工业上,常用惰性电极电解饱和氯化钠溶液制得氯气和烧碱,其电极反应式分别为:阴极
2H++2e-=H2↑
2H++2e-=H2↑
阳极2Cl--2e-=Cl2↑
2Cl--2e-=Cl2↑
;总的电池反应式为2NaCl+2H2O
H2↑+Cl2↑+2NaOH
| ||
2NaCl+2H2O
H2↑+Cl2↑+2NaOH
.
| ||
分析:①若电解质溶液是硫酸铜溶液,铁易失电子发生氧化反应而作负极,铜作正极,正极上得电子发生还原反应;
②用惰性电极电解饱和氯化钠溶液时,阳极上氯离子失电子发生氧化反应,阴极上氢离子失电子发生还原反应,在得失电子相同条件下,将阴阳极电极反应式相加即得电池反应式.
②用惰性电极电解饱和氯化钠溶液时,阳极上氯离子失电子发生氧化反应,阴极上氢离子失电子发生还原反应,在得失电子相同条件下,将阴阳极电极反应式相加即得电池反应式.
解答:解:①该原电池中,铁作负极,负极上铁失电子生成亚铁离子而发生氧化反应,电极反应式为Fe-2e-═Fe2+,铜作正极,正极上铜离子得电子发生还原反应,电极反应式为Cu2++2e-═Cu,
故答案为:负极;Fe-2e-═Fe2+;氧化;正极;Cu2++2e-═Cu;还原;
②用惰性电极电解饱和氯化钠溶液时,阴极上氢离子失电子发生还原反应,电极反应式为2H++2e-=H2↑,阳极上氯离子失电子发生氧化反应,电极反应式为2Cl--2e-=Cl2↑,在得失电子相同条件下,将阴阳极电极反应式相加即得电池反应式,所以电池反应式为2NaCl+2H2O
H2↑+Cl2↑+2NaOH,
故答案为:2H++2e-=H2↑;2Cl--2e-=Cl2↑;2NaCl+2H2O
H2↑+Cl2↑+2NaOH.
故答案为:负极;Fe-2e-═Fe2+;氧化;正极;Cu2++2e-═Cu;还原;
②用惰性电极电解饱和氯化钠溶液时,阴极上氢离子失电子发生还原反应,电极反应式为2H++2e-=H2↑,阳极上氯离子失电子发生氧化反应,电极反应式为2Cl--2e-=Cl2↑,在得失电子相同条件下,将阴阳极电极反应式相加即得电池反应式,所以电池反应式为2NaCl+2H2O
| ||
故答案为:2H++2e-=H2↑;2Cl--2e-=Cl2↑;2NaCl+2H2O
| ||
点评:本题考查了原电池和电解池原理,根据各个电极上得失电子来书写电极反应式,难度不大.

练习册系列答案
相关题目
(12分)如图甲为氢氧燃料电池装置示意图(已标明电池工作时OH-的移动方向),A、B、C、D为电极。
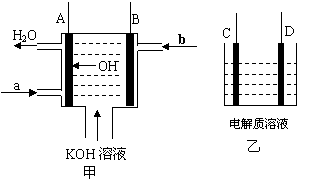 |
(1)若A、B连接外电阻并形成回路,则A电极的电极反应式 ▲ ,b处通入的气体
为 ▲ 。若乙中C为Fe、D石墨,电解质为NaCl,则导线连接C、D后,D电极
的电极反应式 ▲ 。
(2)若乙中C、D均为石墨,电解质溶液为滴有酚酞的NaCl溶液,用导线将A与D相连、
B与C相连,则一段时间后 ▲ 极附近的溶液呈红色,乙中总反应的化学方程式为 ▲_。
(3) 若乙中C为粗铜、D为纯铜片,电解质溶液为硫酸酸化的硫酸铜溶液,用导线将A与
D相连、B与C相连,则乙中D电极的电极反应式 ▲ 。当甲中b气体消耗0.1 mol
时,理论上乙中某电极增重 ▲ g
 (1)(2011?江苏高考,节选)Ag2O2是银锌碱性电池的正极活性物质,其电解质溶液为 KOH 溶液,电池放电时正极的Ag2O2转化为Ag,负极的Zn转化为K2Zn(OH)4,写出该电池反应方程式:
(1)(2011?江苏高考,节选)Ag2O2是银锌碱性电池的正极活性物质,其电解质溶液为 KOH 溶液,电池放电时正极的Ag2O2转化为Ag,负极的Zn转化为K2Zn(OH)4,写出该电池反应方程式:
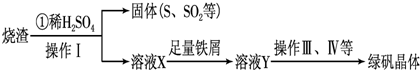
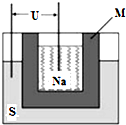 化学反应在工农业生产中有着重要的应用.按要求回答下列问题:
化学反应在工农业生产中有着重要的应用.按要求回答下列问题: