题目内容
已知甲烷的燃烧热为890.3 kJ/mol,氢气的燃烧热为285.8 kJ/mol.现有9 mol的甲烷和氢气的混合气体,完全燃烧后放出热量7408.2 kJ,则该混合气体中碳原子和氢原子的个数比为
- A.1∶8
- B.8∶1
- C.4∶17
- D.17∶4
C
设混合气体中CH4的物质的量为x mol,H2的物质的量为y mol,则有x+y=9,890.3x+285.8y=7408.2.解之得:x=8,y=1,所以原混合气体中C、H原子个数比为8∶(4×8+2×1)=4∶17.
设混合气体中CH4的物质的量为x mol,H2的物质的量为y mol,则有x+y=9,890.3x+285.8y=7408.2.解之得:x=8,y=1,所以原混合气体中C、H原子个数比为8∶(4×8+2×1)=4∶17.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
 2SO3(g)反应过程的能量变化如图所示。已知1mol SO2(g)氧化为1mol的ΔH=—99kJ·mol—1.请回答下列问题:
2SO3(g)反应过程的能量变化如图所示。已知1mol SO2(g)氧化为1mol的ΔH=—99kJ·mol—1.请回答下列问题:
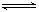 2SO3(g)反应过程的能量变化如图所示。已知1mol SO2(g)氧化为1mol SO3的ΔH=—99kJ·mol—1.请回答下列问题:
2SO3(g)反应过程的能量变化如图所示。已知1mol SO2(g)氧化为1mol SO3的ΔH=—99kJ·mol—1.请回答下列问题: