题目内容
常温下某液态有机物A 10.6g和标况下30LO2完全反应,只生成CO2和液态水,将剩余的气体先通过浓硫酸浓硫酸增重9g,再将剩余的气体通过足量的碱石灰,气体减少17.92L(标况),已知该有机物蒸气相对于相同状况下氢气密度为53.
(1)求该有机物A的分子式(要有计算过程)
(2)又已知该有机物A的核磁共振氢谱中显示有两个峰,且面积之比为3:2.写出A的结构简式并命名.
(1)求该有机物A的分子式(要有计算过程)
(2)又已知该有机物A的核磁共振氢谱中显示有两个峰,且面积之比为3:2.写出A的结构简式并命名.
分析:(1)该有机物蒸气相对于相同状况下氢气密度为53,则该有机物的相对分子质量为53×2=106,浓硫酸质量增重9g为燃烧生成水的质量,将剩余的气体通过足量的碱石灰,气体减少17.92L(标况)为燃烧生成的二氧化碳,根据n=
计算该有机物、水的物质的量,根据n=
计算二氧化碳的物质的量,根据原子守恒计算N(C)、N(H),在结合相对分子质量计算N(O),据此解答;
(2)该有机物A的核磁共振氢谱中显示有两个峰,分子种含有2种H原子,且面积之比为3:2,结合有机物分子式确定其结构,并进行命名.
| m |
| M |
| V |
| Vm |
(2)该有机物A的核磁共振氢谱中显示有两个峰,分子种含有2种H原子,且面积之比为3:2,结合有机物分子式确定其结构,并进行命名.
解答:解:(1)该有机物蒸气相对于相同状况下氢气密度为53,则该有机物的相对分子质量为53×2=106,浓硫酸质量增重9g为燃烧生成水的质量,水的物质的量=
=0.5mol,n(H)=1mol,
将剩余的气体通过足量的碱石灰,气体减少17.92L(标况)为燃烧生成的二氧化碳,其物质的量为
=0.8mol,
10.6g该有机物的物质的量为
=0.1mol,
故该有机物分子中N(C)=
=8、N(H)=
=10,
分子中C、H原子的总的相对原子质量为12×8+10=106,等于该有机物的相对分子质量,故该有机物不含氧元素,故该有机物分子式为C8H10,
答:该有机物分子式为C8H10.
(2)该有机物分子式为C8H10,不饱和度为4,考虑含有苯环,核磁共振氢谱中显示有两个峰,分子种含有2种H原子,且面积之比为3:2,H原子数目分别为6、4,含有2个甲基且处于对位,故其结构简式为 ,为对二甲苯,
,为对二甲苯,
答:该有机物结构简式为 ,名称为对二甲苯.
,名称为对二甲苯.
| 9g |
| 18g/mol |
将剩余的气体通过足量的碱石灰,气体减少17.92L(标况)为燃烧生成的二氧化碳,其物质的量为
| 17.92L |
| 22.4L/mol |
10.6g该有机物的物质的量为
| 10.6g |
| 106g/mol |
故该有机物分子中N(C)=
| 0.8mol |
| 0.1mol |
| 1mol |
| 0.1mol |
分子中C、H原子的总的相对原子质量为12×8+10=106,等于该有机物的相对分子质量,故该有机物不含氧元素,故该有机物分子式为C8H10,
答:该有机物分子式为C8H10.
(2)该有机物分子式为C8H10,不饱和度为4,考虑含有苯环,核磁共振氢谱中显示有两个峰,分子种含有2种H原子,且面积之比为3:2,H原子数目分别为6、4,含有2个甲基且处于对位,故其结构简式为
 ,为对二甲苯,
,为对二甲苯,答:该有机物结构简式为
 ,名称为对二甲苯.
,名称为对二甲苯.点评:本题考查有机物分子式与结构的确定,难度不大,注意掌握燃烧法利用原子守恒确定有机物分子式.

练习册系列答案
相关题目
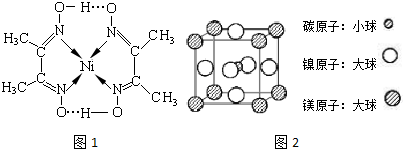
 、④HCHO等,其中碳原子采取sp2杂化的分子有
、④HCHO等,其中碳原子采取sp2杂化的分子有