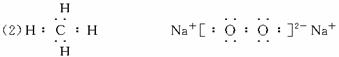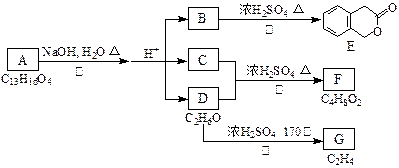题目内容
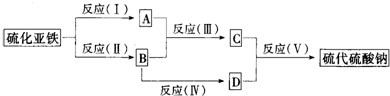
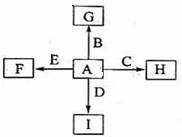 下图中,A、B、C、D、E是单质,G、H、I、F是B、C、D、E分别和A形成的二元化合物。已知:①反应
下图中,A、B、C、D、E是单质,G、H、I、F是B、C、D、E分别和A形成的二元化合物。已知:①反应![]() 能放出大量的热,该反应曾应用于铁轨的焊接;②I是一种常见的温室气体,它和E可以发生反应:
能放出大量的热,该反应曾应用于铁轨的焊接;②I是一种常见的温室气体,它和E可以发生反应:![]() ,F中E元素的质量分数为60%。
,F中E元素的质量分数为60%。
回答问题:⑴①中反应的化学方程式为 ;
⑵化合物I的电子式为 ,它的空间结构是 ;
⑶1.6gG溶于盐酸,得到的溶液与铜粉完全反应,计算至少所需的铜粉的质量(写出离子方程式和计算过程);
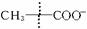
⑷C与过量NaOH溶液反应的离子方程式为 ,反应后溶于与过量化合物I反应的离子方程式为 ;⑸E在I中燃烧观察到的现象是 。
解析:该题有多处“题眼”。依据题目信息C、B是单质,G、H是二元化合物,![]() 反应曾应用于铁轨的焊接,知C为Al、G为Fe2O3、B为Fe、H为Al2O3;由于I是一种常见的温室气体,知其为CO2,而Mg能在CO2中燃烧,且MgO中Mg元素的质量分数为60%。知D为碳单质,A为氧气。
反应曾应用于铁轨的焊接,知C为Al、G为Fe2O3、B为Fe、H为Al2O3;由于I是一种常见的温室气体,知其为CO2,而Mg能在CO2中燃烧,且MgO中Mg元素的质量分数为60%。知D为碳单质,A为氧气。
答案:⑴Al+ Fe2O3![]() Fe+ Al2O3
Fe+ Al2O3
⑵![]()
⑶2Fe3++Cu=2 Fe2++ Cu2+ n(Fe2O3)=0.01mol,依据离子方程式,则n(Cu )= 0.01mol,m(Cu )=0.64g.。
⑷2 Al + 2OH- + 2 H2O=2AlO2- + 3H2↑ AlO2- + CO2 + 2H2O = Al(OH)3↓+ HCO3-
⑸剧烈燃烧,放出热量,生成黑色固体和白色固体。

已知下列数据:
下图为实验室制取乙酸乙酯的装置图。
(1)当饱和碳酸钠溶液上方收集到较多液体时,停止加热,取下小试管B,充分振荡,静置。振荡前后的实验现象_________(填选项)。
| A.上层液体变薄 | B.下层液体红色变浅或变为无色 |
| C.有气体产生 | D.有果香味 |
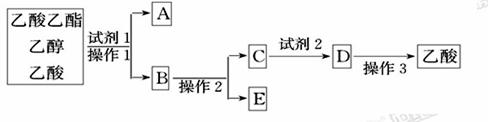
①试剂1最好选用___________;
②操作1是_____,所用的主要仪器名称是________;
③试剂2最好选用___________;
④操作2是___________;
⑤操作3中温度计水银球的位置应为如下图中______(填a、b、c、d)所示,在该操作中,除蒸馏烧瓶、温度计外,还需要的玻璃仪器有_______、_______、_______、______,收集乙酸的适宜温度是___________。