题目内容
研究物质间的氧化还原反应有重要意义.
(1)一定条件下Fe(OH)3与KClO在KOH溶液中反应可制得K2FeO4,其中反应的氧化剂是
(2)高铁电池是一种新型二次电池,电解液为碱溶液,其反应式为:
3Zn(OH)2+2Fe(OH)3+4KOH
3Zn+2K2FeO4+8H2O
放电时电池的负极反应式为
(3)H2O2是一种绿色氧化剂.电解KHSO4溶液制H2O2的原理如下:
①电解池总反应:2SO42-+2H+═S2
+H2↑
②电解生成的S2O82-水解:S2
+2H2O═H2O2+2H++S
.
电解池中阴极反应式
(1)一定条件下Fe(OH)3与KClO在KOH溶液中反应可制得K2FeO4,其中反应的氧化剂是
KClO
KClO
;生成0.1mol K2FeO4转移的电子的物质的量0.3
0.3
mol.(2)高铁电池是一种新型二次电池,电解液为碱溶液,其反应式为:
3Zn(OH)2+2Fe(OH)3+4KOH
| 充电 |
| 放电 |
放电时电池的负极反应式为
Zn+2OH--2e-=Zn(OH)2
Zn+2OH--2e-=Zn(OH)2
.充电时电解液的pH减小
减小
(填“增大”“不变”或“减小”).(3)H2O2是一种绿色氧化剂.电解KHSO4溶液制H2O2的原理如下:
①电解池总反应:2SO42-+2H+═S2
| O | 2- 8 |
②电解生成的S2O82-水解:S2
| O | 2- 8 |
| O | 2- 4 |
电解池中阴极反应式
2H++2e-=H2↑,
2H++2e-=H2↑,
.分析:(1)得电子化合价降低的反应物是氧化剂,根据高铁酸钾和转移电子之间的关系式计算;
(2)负极上锌失电子发生氧化反应,根据溶液中氢氧根离子浓度变化判断;
(3)阴极上氢离子得电子发生还原反应.
(2)负极上锌失电子发生氧化反应,根据溶液中氢氧根离子浓度变化判断;
(3)阴极上氢离子得电子发生还原反应.
解答:解:(1)该反应中,铁元素的化合价由+3价变为+6价,氯元素化合价由+1价变为-1价,所以氢氧化铁是还原剂,次氯酸钾是氧化剂,生成0.1mol K2FeO4转移的电子的物质的量=0.1mol×(6-3)=0.3mol,
故答案为:KClO,0.3;
(2)该原电池放电时,负极上锌失电子和氢氧根离子反应生成氢氧化锌,电极反应式为:Zn+2OH--2e-=Zn(OH)2,充电时,氢氧根离子参加反应生成水,所以随着反应的进行,氢氧根离子浓度减小,溶液的pH减小,故答案为:Zn+2OH--2e-=Zn(OH)2[或3Zn+6OH--6e-=3Zn(OH)2或Zn+2OH-=Zn(OH)2+2e-均合理],减小;
(3)电解时阴极上得电子发生还原反应,根据电池反应式知,氢离子得电子发生还原反应,所以阴极上的电极反应式为:2H++2e-=H2↑,故答案为:2H++2e-=H2↑.
故答案为:KClO,0.3;
(2)该原电池放电时,负极上锌失电子和氢氧根离子反应生成氢氧化锌,电极反应式为:Zn+2OH--2e-=Zn(OH)2,充电时,氢氧根离子参加反应生成水,所以随着反应的进行,氢氧根离子浓度减小,溶液的pH减小,故答案为:Zn+2OH--2e-=Zn(OH)2[或3Zn+6OH--6e-=3Zn(OH)2或Zn+2OH-=Zn(OH)2+2e-均合理],减小;
(3)电解时阴极上得电子发生还原反应,根据电池反应式知,氢离子得电子发生还原反应,所以阴极上的电极反应式为:2H++2e-=H2↑,故答案为:2H++2e-=H2↑.
点评:本题考查原电池和电解池原理及氧化还原反应,明确元素化合价及电极上得失电子是解本题关键,难度不大.

练习册系列答案
 课时训练江苏人民出版社系列答案
课时训练江苏人民出版社系列答案 黄冈经典趣味课堂系列答案
黄冈经典趣味课堂系列答案 启东小题作业本系列答案
启东小题作业本系列答案
相关题目
 3Zn+2K2FeO4+8H2O
3Zn+2K2FeO4+8H2O 3Zn+2K2FeO4+8H2O
3Zn+2K2FeO4+8H2O +2H+═S2
+2H+═S2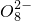 +H2↑
+H2↑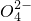 .
.