题目内容
镁条在空气中燃烧生成氧化镁和氮化镁,将燃烧产物溶于60 mL浓度为 2 mol·L-1的盐酸中,以20 mL浓度为0.5 mol·L-1的氢氧化钠溶液中和多余的盐酸,然后在溶液中加入过量的氢氧化钠溶液,并加热使氨气全部挥发,再用稀盐酸吸收氨气,使此盐酸增重0.17 g,求镁条的质量。
〔已知:Mg3N2+6H2O====3Mg(OH)2+2NH3〕
1.2 g
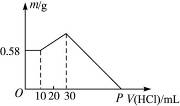
图4-8
解析:
3Mg+N2====Mg3N2
Mg3N2+8HCl====3MgCl2+2NH4Cl
NH4Cl+NaOH![]() NaCl+NH3↑+H2O
NaCl+NH3↑+H2O
3Mg~Mg3N2~8HCl~2NH3
3 8 2
0.015 mol 0.04 mol ![]() =0.01 mol
=0.01 mol
Mg ~ MgO ~ 2HCl
1 2
0.035 mol 0.06 L×2 mol·L-1-0.04 mol-
0.02 L×0.5 mol·L-1=0.07 mol
m(Mg)=(0.015 mol+0.035 mol)×24 g·mol-1=1.2 g
也可采用电荷守恒法。

练习册系列答案
 备战中考寒假系列答案
备战中考寒假系列答案
相关题目
在化学学习与研究中用类推的思维方法有时会产生错误的结论,因此类推的结论最终要经过实践的检验才能确定其正确与否.下列类推结论中正确的是( )
| A、镁条在空气中燃烧生成的氧化物是MgO,则钠在空气中燃烧生成的氧化物是Na2O | B、CO2和SiO2的化学式相似,则CO2与SiO2的物理性质也相似 | C、CO2不能与CaCl2溶液反应,则SO2也不能与CaCl2溶液反应 | D、Na2O中阳、阴离子的个数之比为2:1,可推出Na2O2中阳、阴离子的个数之比为1:1 |
下列说法正确的是( )
| A、Na2O2与水反应,红热的Fe与水蒸气反应均能生成碱 | B、Na和Cs属于第IA族元素,Cs失电子能力比Na强 | C、NaHCO3、Na2CO3、(NH4)2CO3三种固体受热后均能生成气体 | D、镁条在空气中燃烧生成的氧化物是MgO,钠在空气中燃烧生成的氧化物是Na2O |
根据相关的元素化合物的知识,类推得出的结论正确的是( )
| A、镁条在空气中燃烧生成的氧化物是MgO,则钠在空气中燃烧生成的氧化物是Na2O | ||||||||
B、由2Fe+3Cl2
| ||||||||
| C、CO、NO、NO2都是大气污染气体,故在空气中都能稳定存在 | ||||||||
| D、将CO2通入BaCl2溶液不能生成BaCO3,则将SO2通入BaCl2溶液同样不能生成BaSO3 |