题目内容
 水的电离平衡曲线如图所示.下列说法正确的是( )
水的电离平衡曲线如图所示.下列说法正确的是( )| A、水的电离常数KW数值大小关系为:b<c<d |
| B、a点对应的溶液中大量存在:Fe3+、Na+、Cl-、SO42- |
| C、温度不变,加入少量NaOH可使溶液从c点变到 a点 |
| D、在b点对应温度下,将pH=2的HCl与pH=10的NaOH溶液等体积混合后,溶液显中性 |
考点:弱电解质在水溶液中的电离平衡,水的电离
专题:电离平衡与溶液的pH专题
分析:A.依据图象数据分析,纵轴是氢氧根离子浓度,横轴是氢离子浓度,水的离子积常数Kw=c(H+)×c(OH-)计算判断;
B.图象分析a点是常温下的溶液,氢氧根离子浓度和氢离子浓度相等,依据离子性质分析;
C.c、a点是不同温度下的溶液,离子积是随温度变化的;
D.b点Kw=10-12,中性溶液pH=6.
B.图象分析a点是常温下的溶液,氢氧根离子浓度和氢离子浓度相等,依据离子性质分析;
C.c、a点是不同温度下的溶液,离子积是随温度变化的;
D.b点Kw=10-12,中性溶液pH=6.
解答:
解:A.依据图象分析可知,b点Kw=10-12,c点Kw=10-13,d点Kw=10-14,所以b>c>d,故A错误;
B.a点是常温下的溶液,氢氧根离子浓度和氢离子浓度相等,溶液呈中性,a点对应的溶液中大量存在Na+、Cl-、SO42-,但Fe3+、水解显酸性,不符合溶液中性,故B错误;
C.温度不变加入氢氧化钠溶液Kw不变,c、a点是不同温度下的溶液,故C错误;
D.b点Kw=10-12,中性溶液PH=6;将pH=2的HCl与pH=10的NaOH溶液等体积混合后,氢离子浓度和氢氧根离子浓度相同,等体积混合溶液呈中性,故D正确;
故选D.
B.a点是常温下的溶液,氢氧根离子浓度和氢离子浓度相等,溶液呈中性,a点对应的溶液中大量存在Na+、Cl-、SO42-,但Fe3+、水解显酸性,不符合溶液中性,故B错误;
C.温度不变加入氢氧化钠溶液Kw不变,c、a点是不同温度下的溶液,故C错误;
D.b点Kw=10-12,中性溶液PH=6;将pH=2的HCl与pH=10的NaOH溶液等体积混合后,氢离子浓度和氢氧根离子浓度相同,等体积混合溶液呈中性,故D正确;
故选D.
点评:本题考查了水的电离、离子积的概念应用和影响条件,注意离子积常数是随温度变化的,不能根据氢离子浓度确定溶液酸碱性,为易错点.

练习册系列答案
相关题目
有关电化学知识的描述正确的是( )
| A、CaO+H2O═Ca(OH)2,可以放出大量的热,故可把该反应设计成原电池,把其中的化学能转化为电能 |
| B、某原电池反应为Cu+2AgNO3═Cu(NO3)2+2Ag,装置中的盐桥中可以是由KCl饱和溶液制得的琼脂 |
| C、因为铁的活动性强于铜,所以将铁、铜用导线连接后放入浓硝酸中,若能组成原电池,必是铁作负极,铜作正极 |
| D、理论上说,任何能自发进行的氧化还原反应都可被设计成原电池 |
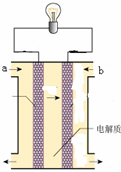 如图所示是一个燃料电池的示意图,当燃料电池如下时,其分析中正确的是( )
如图所示是一个燃料电池的示意图,当燃料电池如下时,其分析中正确的是( )| A、如果a极通入H2,b极通入O2,NaOH溶液作电解质溶液,则通H2的电极上发生的反应为:H2-2e-=2H+ |
| B、如果a极通入H2,b极通入O2,H2SO4溶液作电解质溶液,则通O2的电极上发生的反应为:O2+4e-+2H2O=4OH- |
| C、如果a极通入CH4,b极通入O2,NaOH作电解质溶液,则通CH4的电极上发生的反应为:CH4-8e-+10 OH-=CO32-+7H2O |
| D、如果a极通入H2,b极通入O2,NaOH溶液作电解质溶液,则溶液中的OH-离子向b极附近移动 |
下列说法正确的是( )
| A、SO3溶于水能导电,但SO3是非电解质 |
| B、酸、碱、盐是电解质,都有很强的导电能力 |
| C、电解质在水中一定能导电,在水中导电的化合物一定是电解质 |
| D、纯水的导电性很差,所以水不是电解质 |
对于原电池的电极名称,叙述错误的是( )
| A、发生氧化反应的一极为负极 |
| B、正极为电子流入的一极 |
| C、比较不活泼的金属为负极 |
| D、电流流出的一极为正极 |
下列叙述正确的是( )
| A、将稀氨水逐滴加入稀硫酸中,当溶液的pH=7时,c(SO42-)>c(NH4+) | ||
| B、两种醋酸溶液的物质的量浓度分别为c1和c2,pH分别为a和a+1,则c1=10c2 | ||
| C、pH=13的NaOH溶液与pH=1的醋酸溶液等体积混合,滴入石蕊溶液呈红色 | ||
D、向0.1mol?L-1的氨水中加入少量硫酸铵固体,则溶液中
|
N2O5是一种新型硝化剂,在一定温度下可发生以下反应:2N2O5(g)?4NO2(g)+O2(g)△H>0,T1温度时,向密闭容器中通入N2O5,部分实验数据见表格,下列说法中不正确的是( )
| 时间/s | 0 | 500 | 1000 | 1500 | ||
|
5.00 | 3.52 | 2.50 | 2.50 |
| A、500s内N2O5分解速率为2.96×10-3mol?L-1?s-1 | ||
| B、T1温度下的平衡常数为K1=125,平衡时N2O5的转化率为50% | ||
| C、T1温度下的平衡常数为K1,T2温度下的平衡常数为K2,若T1>T2,则K1<K2 | ||
D、达平衡后其他条件不变,将容器的体积压缩到原来的
|