题目内容
将15mL 2mol-L-1 Na2CO3溶液逐滴加入到40mL 0.5mol-L-1 MCln盐溶液中,恰好将溶液中的Mn+离子完全沉淀为碳酸盐,则MCln中n值是( )
| A.4 | B.3 | C.2 | D.1 |
Na2CO3溶液中nCO32-离子的物质的量为15mL×10-3×2mol?L-1=0.03mol,
MCln盐溶液中Mn+离子的物质的量为40mL×10-3×0.5mol?L-1=0.02mol,
由反应中恰好将溶液中的Mn+离子完全沉淀为碳酸盐,及M的化合价为+n,
则Na2CO3与MCln反应对应的关系式为:
2Mn+~nCO32-
2 n
0.02mol 0.03mol
=
,解得n=3,
故选:B.
MCln盐溶液中Mn+离子的物质的量为40mL×10-3×0.5mol?L-1=0.02mol,
由反应中恰好将溶液中的Mn+离子完全沉淀为碳酸盐,及M的化合价为+n,
则Na2CO3与MCln反应对应的关系式为:
2Mn+~nCO32-
2 n
0.02mol 0.03mol
| 2 |
| n |
| 0.02mol |
| 0.03mol |
故选:B.

练习册系列答案
相关题目

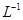
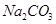 溶液逐滴加入到40 ml.0.5mol•.
溶液逐滴加入到40 ml.0.5mol•.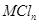 盐溶液中,恰好将溶液中的
盐溶液中,恰好将溶液中的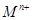 离子完全沉淀为碳酸盐,则
离子完全沉淀为碳酸盐,则
