��Ŀ����
������ͼ��ʾװ�ú����������������ش��й����⣮
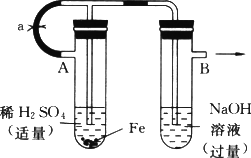
����ͼ��ʾװ�ã������ֲ�ͬ�IJ��������ֱ����ʵ�飬�۲�B���е�����
(1)�������ȼн�ֹˮ��a����ʹA�ܿ�ʼ��Ӧ��ʵ����B���й۲쵽��������________���йط�Ӧ�����ӷ���ʽ��________��
(2)������ֹˮ��a��ʹA�ܷ�Ӧһ��ʱ����ټн�ֹˮ��a��ʵ����B���й۲쵽��������________���йط�Ӧ�����ӷ���ʽ��________��
(3)��˵�������������ͬ��ԭ��(������������ͬ����С�ⲻ�ûش�)________��
������
����
���������������Ǹ���Fe(OH)2��ʵ�����Ʒ���Ƶģ�����Fe(OH)2���ױ�����ΪFe(OH)3����Һ���ܽ���������ܰ������������н�aʱ��A�Թܱ����һ�������ϵ������������ʹA�Թ���ѹǿ�������ɵ�FeSO4��Һѹ��B�У��Ӷ�������Ӧ����Fe(OH)2���ɣ���NaOH��Һ���ܽ�������ɽ�Fe(OH)2Ѹ�����������ת���Fe(OH)3�����Կ�����ɫ������ʱ��̣ܶ����ò�����ʱ��������H2����ͨ��������ͨ�뵽B�е�NaOH��Һ�У��������ܽ��O2���ߣ��ټн�aʱ��FeSO4��Һѹ��B�У���ʱ��Ӧ��������Fe(OH)2��һ��ʱ���ڲ���ɫ��
��ʾ��
����ܽϳ�ʱ�俴��Fe(OH)2��ɫ������ʵ�飬ע�����֪ʶ�����Ӧ�ã���Ҫ�Ƿ�ֹ������

 ��2009?�Ͼ���ģ��ijͬѧ��Cu��HNO3�ķ�Ӧ��������̽������ش��й����⣮
��2009?�Ͼ���ģ��ijͬѧ��Cu��HNO3�ķ�Ӧ��������̽������ش��й����⣮ ��2010?���ֶ�ģ��ij����ʵ��С���������ͼ��ʾװ�ý��С�һ�����á���ʵ��̽�����г�װ������ȥ����
��2010?���ֶ�ģ��ij����ʵ��С���������ͼ��ʾװ�ý��С�һ�����á���ʵ��̽�����г�װ������ȥ���� ijͬѧ��������װ��ʵ��ͭ��Ũ���ᡢϡ���ᷴӦ��������ͼ��ʾ��
ijͬѧ��������װ��ʵ��ͭ��Ũ���ᡢϡ���ᷴӦ��������ͼ��ʾ�� ��2012?������һģ����Դ��ȱ������������ٵ��ش����⣮�״���һ�ֿ�������Դ�����й㷺�Ŀ�����Ӧ��ǰ����
��2012?������һģ����Դ��ȱ������������ٵ��ش����⣮�״���һ�ֿ�������Դ�����й㷺�Ŀ�����Ӧ��ǰ����

