题目内容
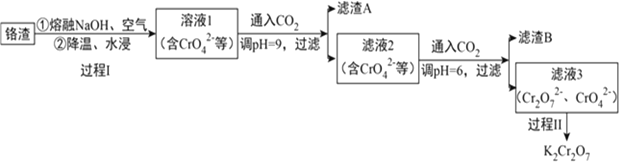
【题目】利用熔融碱焙烧工艺可从铝热法生产金属铬的铬渣(Al、Al2O3、Cr2O3等)中浸出铬和铝,为实现铬和铝的再生利用。其工作流程如下:
(1)铝热法冶炼金属铬,是利用了金属铝的__________(填“氧化性”或“还原性”)。
(2)溶液1中的阴离子有CrO42-、______、_______。
(3)过程I,在Cr2O3参与的反应中,若生成0.4molCrO42-,消耗氧化剂的物质的量是_______。
(4)通入CO2调节溶液pH实现物质的分离。
①滤渣A煅烧得到Al2O3,再用电解法冶炼Al。冶炼Al的化学方程式是____________________。
②滤渣B受热分解所得物质可以循环利用,B是__________。
③已知:2CrO42-+2H+ ![]() Cr2O72-+H2O K=4.0×1014滤液3中Cr2O72-的浓度是0.04mol/L,则CrO42-的浓度是__________mol/L。
Cr2O72-+H2O K=4.0×1014滤液3中Cr2O72-的浓度是0.04mol/L,则CrO42-的浓度是__________mol/L。
(5)过程II的目的是得到K2Cr2O7粗品。下表是不同温度下化合物的溶解度(g/100gH2O)
化合物名称 | 0℃ | 20℃ | 40℃ | 60℃ | 80℃ |
NaCl | 35.7 | 36.0 | 36.6 | 373 | 38.4 |
KCl | 28.0 | 34.2 | 40.1 | 45.8 | 51.3 |
K2Cr2O7 | 4.7 | 12.3 | 26.3 | 45.6 | 73.0 |
Na2Cr2O7 | 163 | 183 | 215 | 269 | 376 |
结合表中数据分析,过程II的操作是:向滤液③中加入稀盐酸和KCl固体后,_____________,过滤,得到K2Cr2O7粗品。
【答案】还原性 AlO2- OH- 0.3mol 2Al2O3(熔融) 3O2↑+4Al NaHCO3 0.01 蒸发浓缩、降温结晶
3O2↑+4Al NaHCO3 0.01 蒸发浓缩、降温结晶
【解析】
利用熔融碱焙烧工艺可从铝热法生产金属铬所得铬渣(Al、Al2O3、Cr2O3等)中浸出铬和铝,铬渣加入熔融NaOH、空气,降温水浸,铝、氧化铝溶解生成偏铝酸钠,Cr2O3溶解得到CrO42-,得到溶液Ⅰ中含有CrO42-、AlO2-、OH-,通入二氧化碳调节溶液pH=9沉淀铝离子生成氢氧化铝沉淀,滤渣A为氢氧化铝,滤液2继续通入二氧化碳调节溶液pH=6过滤得到,滤渣B为碳酸氢钠晶体,滤液3含Cr2O72-、CrO42-等,过程Ⅱ的目的是得到K2Cr2O7粗品,粗品再重结晶可制得纯净的K2Cr2O7,
(1)铝热反应中铝失电子作还原剂。
(2)铝、氧化铝溶解生成偏铝酸钠,Cr2O3溶解得到CrO42-,得到溶液Ⅰ中含有CrO42-、AlO2-、OH-。
(3)在Cr2O3参与的反应中,若生成0.4mol CrO42-,反应的离子方程式为:2Cr2O3+8OH-+3O2=4CrO42-+4H2O,据此计算,反应的氧化剂氧气物质的量为0.3mol;
(4)①电解熔融氧化铝生成铝和氧气,化学方程式为2Al2O3(熔融) 3O2↑+4Al。
3O2↑+4Al。
②滤渣B受热分解所得物质可以循环利用是碳酸氢钠分解生成的碳酸钠,B为碳酸氢钠晶体。
③已知:2CrO42-+2H+=Cr2O72-+H2O K=4.0×1014,滤液3中Cr2O72-的浓度是0.04mol/L,K=![]() ,氢离子浓度c(H+)=10-6mol/L,CrO42-的浓度=
,氢离子浓度c(H+)=10-6mol/L,CrO42-的浓度=![]() ,经计算得c =
,经计算得c = ![]() 。
。
(5)过程Ⅱ得到K2Cr2O7粗品是溶液中得到溶质固体,利用物质溶解度分析,K2Cr2O7溶解度比Na2Cr2O7 小,加入氯化钾和稀盐酸蒸发浓缩、降温结晶得到晶体。

 每日10分钟口算心算速算天天练系列答案
每日10分钟口算心算速算天天练系列答案