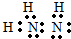题目内容
(1)下列括号内的物质为杂质,将除去下列各组混合物中杂质所需的试剂填写在横线上:
乙烷(乙烯)______; 苯(苯酚)______;
乙酸乙酯(乙酸)______;溴苯(溴)______.
(2)下列5种有机化合物:乙酸乙酯(CH3COOCH2CH3)、苯酚( )、乙醛(CH3CHO)、乙酸(CH3COOH)、乙醇(CH3CH2OH).
)、乙醛(CH3CHO)、乙酸(CH3COOH)、乙醇(CH3CH2OH).
①其中能与NaHCO3溶液反应产生气泡的是______.
②其中能与FeCl3溶液发生显色反应的是______.
③其中能发生水解反应的是______.
④写出乙醛与银氨溶液发生银镜反应的化学方程式______.
解:(1)因乙烷不与溴水反应,乙烯与溴水反应,则除去乙烷中的乙烯选择溴水;
因苯与NaOH溶液不反应,苯酚与NaOH溶液反应,则除去苯中的苯酚选择NaOH溶液;
乙酸乙酯不与碳酸钠溶液不反应,乙酸与碳酸钠溶液反应,则除去乙酸乙酯中的乙酸,选择碳酸钠溶液;
因溴苯与NaOH不反应,溴与NaOH溶液反应,则除去溴苯中的溴选择NaOH溶液,
故答案为:溴水;NaOH溶液;饱和碳酸钠溶液;NaOH溶液;
(2)①具有酸性的物质能与NaHCO3溶液反应,酸性乙酸>HCO3->苯酚,则以上几种物质只有乙酸与NaHCO3溶液反应产生气泡,故答案为:乙酸(CH3COOH);
②以上几种物质中只有苯酚遇FeCl3溶液发生显色反应,故答案为:苯酚;
③上述几种物质中只有乙酸乙酯能发生水解,故答案为:乙酸乙酯(CH3COOCH2CH3);
④乙醛与银氨溶液发生银镜反应生成醋酸铵、Ag、氨气、水,该反应为CH3CHO+2Ag(NH3)OH CH3COONH4+2Ag↓+3NH3+H2O,
CH3COONH4+2Ag↓+3NH3+H2O,
故答案为:CH3CHO+2Ag(NH3)OH CH3COONH4+2Ag↓+3NH3+H2O.
CH3COONH4+2Ag↓+3NH3+H2O.
分析:(1)除杂的原则不能引入新的杂质,不能与被除杂的物质发生化学反应,结合物质的性质来分析除杂;
(2)①具有酸性的物质能与NaHCO3溶液反应,酸性乙酸>HCO3->苯酚;
②苯酚遇FeCl3溶液发生显色反应;
③上述几种物质中只有乙酸乙酯能发生水解;
④乙醛与银氨溶液发生银镜反应生成醋酸铵、Ag、氨气、水.
点评:本题考查混合物的分离、提纯,明确除杂的原则及物质的性质、分离提纯的方法是解答本题的关键,题目难度不大.
因苯与NaOH溶液不反应,苯酚与NaOH溶液反应,则除去苯中的苯酚选择NaOH溶液;
乙酸乙酯不与碳酸钠溶液不反应,乙酸与碳酸钠溶液反应,则除去乙酸乙酯中的乙酸,选择碳酸钠溶液;
因溴苯与NaOH不反应,溴与NaOH溶液反应,则除去溴苯中的溴选择NaOH溶液,
故答案为:溴水;NaOH溶液;饱和碳酸钠溶液;NaOH溶液;
(2)①具有酸性的物质能与NaHCO3溶液反应,酸性乙酸>HCO3->苯酚,则以上几种物质只有乙酸与NaHCO3溶液反应产生气泡,故答案为:乙酸(CH3COOH);
②以上几种物质中只有苯酚遇FeCl3溶液发生显色反应,故答案为:苯酚;
③上述几种物质中只有乙酸乙酯能发生水解,故答案为:乙酸乙酯(CH3COOCH2CH3);
④乙醛与银氨溶液发生银镜反应生成醋酸铵、Ag、氨气、水,该反应为CH3CHO+2Ag(NH3)OH
 CH3COONH4+2Ag↓+3NH3+H2O,
CH3COONH4+2Ag↓+3NH3+H2O,故答案为:CH3CHO+2Ag(NH3)OH
 CH3COONH4+2Ag↓+3NH3+H2O.
CH3COONH4+2Ag↓+3NH3+H2O.分析:(1)除杂的原则不能引入新的杂质,不能与被除杂的物质发生化学反应,结合物质的性质来分析除杂;
(2)①具有酸性的物质能与NaHCO3溶液反应,酸性乙酸>HCO3->苯酚;
②苯酚遇FeCl3溶液发生显色反应;
③上述几种物质中只有乙酸乙酯能发生水解;
④乙醛与银氨溶液发生银镜反应生成醋酸铵、Ag、氨气、水.
点评:本题考查混合物的分离、提纯,明确除杂的原则及物质的性质、分离提纯的方法是解答本题的关键,题目难度不大.

练习册系列答案
 学而优衔接教材南京大学出版社系列答案
学而优衔接教材南京大学出版社系列答案 小学课堂作业系列答案
小学课堂作业系列答案 金博士一点全通系列答案
金博士一点全通系列答案
相关题目
物质的分离提纯:
(1)下列各组混和物的分离提纯或是检验应采用什么方法?
①实验室中的石灰水久置,液面上常悬浮有CaCO3微粒.可用______的方法除去Ca(OH)2溶液中悬浮的CaCO3微粒.
②鉴别胶体和溶液的一般方法是______.
③除去乙醇中溶解的微量食盐可采用______的方法.
④从碘水中提取碘可采用______的方法.
⑤除去氧化钙中的碳酸钙可用______的方法.
(2)填表.
| 混合物(括号内为杂质) | 提纯用试剂 | 发生反应的离子方程式 |
| Na2SO4(MgSO4) | ______ | ______ |
| KOH(Ba(OH)2) | ______ | ______ |
| NaCl(NaOH和Na2CO3) | ______ | ______ |
物质的分离提纯:
(1)下列各组混和物的分离提纯或是检验应采用什么方法?
①实验室中的石灰水久置,液面上常悬浮有CaCO3微粒.可用______的方法除去Ca(OH)2溶液中悬浮的CaCO3微粒.
②鉴别胶体和溶液的一般方法是______.
③除去乙醇中溶解的微量食盐可采用______的方法.
④从碘水中提取碘可采用______的方法.
⑤除去氧化钙中的碳酸钙可用______的方法.
(2)填表.
(1)下列各组混和物的分离提纯或是检验应采用什么方法?
①实验室中的石灰水久置,液面上常悬浮有CaCO3微粒.可用______的方法除去Ca(OH)2溶液中悬浮的CaCO3微粒.
②鉴别胶体和溶液的一般方法是______.
③除去乙醇中溶解的微量食盐可采用______的方法.
④从碘水中提取碘可采用______的方法.
⑤除去氧化钙中的碳酸钙可用______的方法.
(2)填表.
| 混合物(括号内为杂质) | 提纯用试剂 | 发生反应的离子方程式 |
| Na2SO4(MgSO4) | ______ | ______ |
| KOH(Ba(OH)2) | ______ | ______ |
| NaCl(NaOH和Na2CO3) | ______ | ______ |