题目内容
用下面的方法可以制得较纯净的Na2CO3溶液,并能较准确地测得Na2CO3固体的纯度。Ⅰ.制备Na2CO3溶液
操作步骤:①将50mLNaOH溶液等分为两份;
②用其中一份溶液吸收过量的CO2气体,至CO2气体不再溶解;
③小火煮沸溶液1—2分钟,除去过量溶解的CO2气体;
④在得到的溶液中加入另一半NaOH溶液,使其充分反应。
(1)以上制备原理为(用化学方程式表示)______________________________;
(2)若将步骤③,④的顺序对调,即先混合再煮沸,合理吗?__________;理由是______________________________。
Ⅱ.测定Na2CO3固体的纯度(杂质不与水或酸反应)
所用装置:

操作步骤:
①按上图所示,组装好实验仪器,并检查其气密性;
②准确称量U形管D(包括内盛物质)的质量(设为m
③准确称量一定量的Na2CO3样品(设为n g),并将其放进B瓶内;
④从分液漏斗中缓缓滴入一定量H2SO4,并从a处缓缓鼓入空气,至B反应器中不再产生气体为止;
⑤准确称量U形管D(包括内盛物质)的总质量(设为m
(设原容器中所含CO2气体可忽略不计,各容器内反应完全)
(1)从a处缓缓鼓入空气的作用是__________________________________;
(2)装置A中盛装的液体为__________,装置A的作用是__________________________;
如果撤去装置A,直接向装置B中缓缓鼓入空气,则会导致实验测定结果__________;
(3)装置C中盛装的液体为__________,装置C的作用是__________;如果撤去装置C,则会导致实验测定结果__________;
(4)装置E的作用是__________;
(5)Na2CO3样品中Na2CO3的质量分数是__________(用m1、m2、n表示)。
Ⅰ.(1)NaOH+CO2![]() NaHCO3
NaHCO3
NaHCO3+NaOH![]() Na2CO3+H2O
Na2CO3+H2O
(2)不合理 溶液中溶解的CO2又能和NaOH反应,NaHCO3不能反应完全
Ⅱ.(1)使B中产生的气体被D完全吸收
(2)NaOH溶液 吸收空气中的CO2 偏高
(3)浓H2SO4 吸收水蒸气 偏高
(4)防止空气中的CO2和水蒸气被D吸收
(5)![]() ×100%
×100%
【解析】本题考查物质制备和定量测定实验,中等题。Ⅰ(1)制备原理为:NaOH![]() NaHCO3
NaHCO3![]() Na2CO3;(2)颠倒,则溶解的CO2能与NaOH反应使得NaHCO3不能反应完全。Ⅱ测定原理是通过碱石灰(D)的增重,确定产生的CO2,结合混合物的质量进行计算,(1)a的作用是使产生的CO2被D全部吸收;(2)装置A盛装NaOH是为了吸收空气中的CO2,直接鼓入空气,则产生的CO2偏大,Na2CO3的含量偏大。(3)装置C盛装浓硫酸,吸收产生的水蒸气,撤去C,则产生的CO2偏大,Na2CO3的含量偏大。(4)装置E是为了防止空气中的CO2和H2O进入装置。(5)CO2的质量为:(m2-m1)g,则Na2CO3的质量为:
Na2CO3;(2)颠倒,则溶解的CO2能与NaOH反应使得NaHCO3不能反应完全。Ⅱ测定原理是通过碱石灰(D)的增重,确定产生的CO2,结合混合物的质量进行计算,(1)a的作用是使产生的CO2被D全部吸收;(2)装置A盛装NaOH是为了吸收空气中的CO2,直接鼓入空气,则产生的CO2偏大,Na2CO3的含量偏大。(3)装置C盛装浓硫酸,吸收产生的水蒸气,撤去C,则产生的CO2偏大,Na2CO3的含量偏大。(4)装置E是为了防止空气中的CO2和H2O进入装置。(5)CO2的质量为:(m2-m1)g,则Na2CO3的质量为:![]() ×106=
×106=![]() g,故Na2CO3的含量为:
g,故Na2CO3的含量为: ×100%=
×100%=![]() ×100%。
×100%。

 33、用下面两种方法可以制得白色的Fe(OH)2沉淀.
33、用下面两种方法可以制得白色的Fe(OH)2沉淀.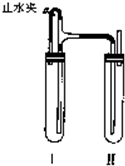 (2011?佛山二模)用下面两种方法可以制得白色的Fe(OH)2沉淀.
(2011?佛山二模)用下面两种方法可以制得白色的Fe(OH)2沉淀.