��Ŀ����
ƽ�ⳣ��KC����ֵ��С���Ǻ�����ѧ��Ӧ���г̶ȵı�־����25��ʱ�����з�Ӧ��ƽ�ⳣ�����£�
N2(g) + O2(g) ![]() 2NO(g) K1 = 1��10��30
2NO(g) K1 = 1��10��30
2H2(g) + O2(g) ![]() 2H2O(g) K2 = 2��10 81
2H2O(g) K2 = 2��10 81
2CO2 (g) ![]() 2CO(g)��O2(g) K3 = 4��10��92
2CO(g)��O2(g) K3 = 4��10��92
��1�������£�NO�ֽ����O2��Ӧ��ƽ�ⳣ���ı���ʽΪK = ��
��2�������£�ˮ�ֽ����O2����ʱƽ�ⳣ��ֵԼΪK = ��
��3�������£�NO��H2O��CO2 ���ֻ�����ֽ�ų������������С˳��Ϊ ��
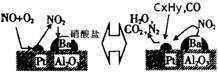
��4������������Ҫ��ȫ�ж�����β������װ����ɸ�װ����������ϳ�ȥ�������һ����̼��Ⱦ������ŷţ�����װ���β������װ����Ҫ�Ǽ�����Ч����������������й����ݷ�������ʹ�ô�������Ⱦ����Ŀ����ԡ�
��1��K=![]() ��2��5��10��82 ��3��NO��H2O��CO2
��2��5��10��82 ��3��NO��H2O��CO2
��4��NO��CO��O2��Ӧ���еij̶Ⱥܴ�ʹ�ú��ʵĴ����ӿ췴Ӧ���ʣ���ˮ��������������HNO3��CO2��������Ͽ��Գ�ȥ��Ⱦ���塣 ���ɵ�1��3����Ӧ��ƽ�ⳣ����֪2CO + 2NO=2CO2 + N2��K = 1/K1K2 = 2.5��10121��ʹ�ú��ʵĴ����ӿ췴Ӧ���ʣ������Ͽ��Գ�ȥ��Ⱦ���塣

 ��ʦ����ָ���ο�ʱϵ�д�
��ʦ����ָ���ο�ʱϵ�д���ѧƽ�ⳣ��K����ֵ��С�Ǻ�����ѧ��Ӧ���г̶ȵı�־���ڳ����£����з�Ӧ��ƽ�ⳣ������ֵ���£�
2NO(g)  N2(g)��O2(g)��K1��1��1030
N2(g)��O2(g)��K1��1��1030
2H2(g)��O2(g)  2H2O(g)��K2��2��1081
2H2O(g)��K2��2��1081
2CO2(g)  2CO(g)��O2(g)��K3��4��10��92
2CO(g)��O2(g)��K3��4��10��92
����˵����ȷ����
| A�������£�NO�ֽ����O2�ķ�Ӧ��ƽ�ⳣ������ʽΪK1��c(N2)��c(O2) |
| B�������£�ˮ�ֽ����O2����ʱƽ�ⳣ������ֵԼΪ5��10��80 |
| C�������£�NO��H2O��CO2�������ʷֽ�ų�O2�������ɴ�С��˳��Ϊ NO��H2O��CO2 |
| D������˵��������ȷ |
 2NO(g) K1��1��10��30 ��
2NO(g) K1��1��10��30 �� �ٳ����£���Ӧ2H2O(g)
2H2(g) +O2(g) ƽ�ⳣ��K�� ��
�ٳ����£���Ӧ2H2O(g)
2H2(g) +O2(g) ƽ�ⳣ��K�� �� N2(g)��O2(g)��K1��1��1030
N2(g)��O2(g)��K1��1��1030 2H2O(g)��K2��2��1081
2H2O(g)��K2��2��1081