题目内容
【题目】常温下,0.1molL-1某一元酸(HA)溶液![]() 中= 1×10-8,相同物质的量浓度的某一元碱(BOH)溶液中
中= 1×10-8,相同物质的量浓度的某一元碱(BOH)溶液中![]() = 1×1012,下列叙述正确的是( )
= 1×1012,下列叙述正确的是( )
A.PH=a的HA溶液,稀释10倍,其pH=a+1
B.等体积的HA和BOH恰好完全反应,溶液的pH=7
C.HA的pH=3;BOH的pH=13
D.相同体积相同pH的HA和盐酸分别与足量Zn反应,生成氢气的物质的量相同
【答案】C
【解析】
试题分析:A.根据A可知.0.1molL-1某一元酸(HA)溶液的pH=3,说明HA为弱酸,稀释后电离程度增大,溶液中氢离子浓度增大,则溶液的pH小于a+1,故A错误;B.0.1molL-1的BOH溶液的pH=13,说明BOH为强电解质,两溶液等体积混合后生成强碱弱酸盐,溶液显示碱性,故B错误;C.常温下,溶液中![]() =1×10-8、Kw=c(H+)c(OH-)=1×10-14,联立解得c(H+)=10-3mol/L,该溶液的pH=3;联立
=1×10-8、Kw=c(H+)c(OH-)=1×10-14,联立解得c(H+)=10-3mol/L,该溶液的pH=3;联立![]() =1×1012、Kw=c(H+)c(OH-)=1×10-14解得:c(OH-)=10-1mol/L,该溶液的pH=13,故C正确;D.HA为弱酸,在溶液中只能部分电离出氢离子,pH相等的HA和盐酸中,HA的物质的量浓度大于盐酸,则相同体积相同pH的HA和盐酸分别与足量Zn反应,HA产生的氢气多,故D错误;故选C。
=1×1012、Kw=c(H+)c(OH-)=1×10-14解得:c(OH-)=10-1mol/L,该溶液的pH=13,故C正确;D.HA为弱酸,在溶液中只能部分电离出氢离子,pH相等的HA和盐酸中,HA的物质的量浓度大于盐酸,则相同体积相同pH的HA和盐酸分别与足量Zn反应,HA产生的氢气多,故D错误;故选C。

 探究与巩固河南科学技术出版社系列答案
探究与巩固河南科学技术出版社系列答案【题目】下图中a、b分别是原电池的两极,接通电路后发现a极板质量增加,b极板溶解,符合这一情况的是( )
a极板 | b极板 | a电极 | Z溶液 | |
A | 锌 | 石墨 | 负极 | CuSO4 |
B | 石墨 | 石墨 | 负极 | NaOH |
C | 银 | 铁 | 正极 | AgNO3 |
D | 铜 | 石墨 | 正极 | CuCl2 |

A. A B. B C. C D. D
【题目】Ⅰ.高纯度氢氧化镁广泛应用于医药、电力等领域。镁硅酸盐矿石可用于生产氢氧化镁,简要工艺流程如图所示:
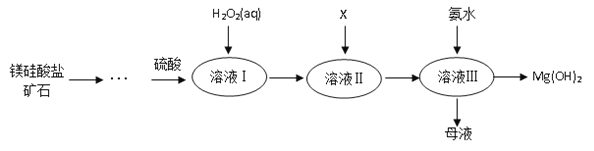
已知:
①溶液Ⅰ中除含Mg2+、SO42外,还含有少量Fe3+、Al3+、Fe2+等离子;
②常温下,几种金属离子开始沉淀和沉淀完全时的pH如下表所示:
金属离子 | Fe3+ | Al3+ | Fe2+ | Mg2+ |
开始沉淀时的pH | 1.5 | 3.3 | 6.5 | 9.4 |
沉淀完全时的pH | 3.7 | 5.2 | 9.7 | 12.4 |
请回答下列问题:
(1)镁在元素周期表中的位置_______________;
(2)向溶液Ⅱ中加入试剂X是_____________,作用是_________________________;
(3)流程中不加H2O2引起的后果是___________________________________;
(4)说出母液的一种用途___________________;
(5)加入H2O2溶液发生反应的离子方程式是___________________;
Ⅱ.海水中含有丰富的镁资源。某同学设计了从模拟海水中制备MgO的实验方案:
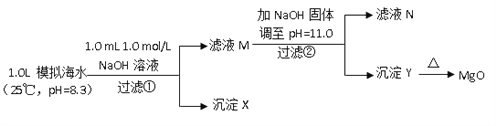
模拟海水中的离子浓度/ (mol/L) | Na+ | Mg2+ | Ca2+ | Cl- | HCO3- |
0.439 | 0.050 | 0.011 | 0.560 | 0.001 |
注:溶液中某种离子的浓度小于1.0×10-5mol/L,可认为该离子不存在;实验过程中,假设溶液体积不变。
已知:Ksp(CaCO3)=4.96×10-9;Ksp(MgCO3)=6.82×10-6;Ksp [Ca(OH)2]=4.68×10-6;Ksp [Mg(OH)2]=5.61×10-12。请回答下列问题:
(6)沉淀物X为_____________;
(7)滤液N中Ca2+浓度为_______________;
(8)加NaOH固体调整pH=12.5是否可行______(填“是”“否”);原因是________。