题目内容
Ⅰ)如图所示,甲、乙之间的隔板K和活塞F都可左右移动,甲中充入2molA和1molB,乙中充入2molC和1molHe,此时K停在0处。在一定条件下发生可逆反应:2A(g)+B(g)![]() 2C(g);反应达到平衡后,再恢复至原温度。回答下列问题:
2C(g);反应达到平衡后,再恢复至原温度。回答下列问题:
(1)可根据 现象来判断甲、乙都已达到平衡。
(2)达到平衡时,隔板K最终停留在0刻度左侧a处,

则a的取值范围是 (3)若达到平衡时,隔板K最终停留在左侧刻度1处,则甲中C的物质的量为 mol,乙中C的转化率 ______50%(填:>、<、=),此时,乙中可移动活塞F最终停留在右侧刻度 处(填下列序号)① <6 ② >6 ③ =6。
(4)若达到平衡时,隔板K最终停留在左侧刻度靠近0处,则乙中可移动活塞F最终停留在右侧的刻度不大于 ;若K最终停留在左侧刻度靠近2处,则乙中F最终停留在右侧的刻度不小于 。
(Ⅱ)若一开始就将K、F固定,其他条件均不变,则达到平衡时:
(1)甲、乙中C的摩尔分数是 (填:“甲>乙”或“甲<乙”或“甲=乙” );
(2)测得甲中A的转化率为b,则乙中C的转化率为 ;
(3)假设乙、甲两容器中的压强比用d表示,则d的取值范围是 。
【解析】该题涉及化学反应速率和化学反应限度的有关问题的讨论和化学平衡移动原理的应用,是近几年高考中常考的题型之一。
【答案】(Ⅰ)(1)K、F不再移动
(2)0<a<2
(3)1 > ② (4)8 4
(Ⅱ)(1)甲=乙 (2)1-b (3)![]() <d<
<d<![]()

 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案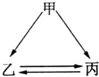 如图所示的甲、乙、丙三种物质均含有相同的某种元素,箭头表示物质间的转化一步就能实现,则甲可能是( )
如图所示的甲、乙、丙三种物质均含有相同的某种元素,箭头表示物质间的转化一步就能实现,则甲可能是( )①C ②H2O2 ③Na ④Fe ⑤HNO3.
| A、仅①③④ | B、仅①②⑤ | C、仅①②③⑤ | D、①②③④⑤ |
 分别回答下列问题.
分别回答下列问题.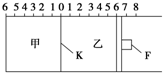 如图所示,甲、乙之间的隔板K和活塞F都可左右移动,甲中充入2mol SO2和1mol O2,乙中充入2mol SO3和1mol He,此时K停在0处.在一定条件下发生可逆反应:2SO2(g)+O2(g)?2SO3(g),反应达到平衡后,再恢复至原温度.回答下列问题:
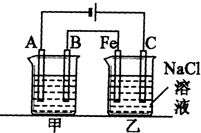
如图所示,甲、乙之间的隔板K和活塞F都可左右移动,甲中充入2mol SO2和1mol O2,乙中充入2mol SO3和1mol He,此时K停在0处.在一定条件下发生可逆反应:2SO2(g)+O2(g)?2SO3(g),反应达到平衡后,再恢复至原温度.回答下列问题: 如图所示,甲、乙两池电极材料都是铁棒和碳棒,请回答下列问题:
如图所示,甲、乙两池电极材料都是铁棒和碳棒,请回答下列问题: