题目内容
【题目】烃的衍生物有多种,按要求回答下列问题:
(1)若分子式为C4H10O并能与金属钠反应放出H2的有机化合物有________种。
(2)与化合物C7H10O2互为同分异构体的物质不可能为________(填序号)。
A.醇 B.醛 C.羧酸 D.酚
(3)与![]() 具有相同官能团的同分异构体的结构简式为______________(写出一种即可)。
具有相同官能团的同分异构体的结构简式为______________(写出一种即可)。
(4)苯氧乙酸(![]() )有多种酯类的同分异构体。其中能与FeCl3溶液发生显色反应,且苯环上有2种一硝基取代物的同分异构体是________(写出任意两种的结构简式)。
)有多种酯类的同分异构体。其中能与FeCl3溶液发生显色反应,且苯环上有2种一硝基取代物的同分异构体是________(写出任意两种的结构简式)。
(5)分子式为C5H10的烯烃共有(不考虑顺反异构)__________种。
【答案】4 D CH2=CHCH2COOH或CH3CH=CHCOOH ![]() 、
、![]() 、
、![]() (任写两种) 5
(任写两种) 5
【解析】
(1)分子式为C4H10O并能与金属钠反应放出氢气,则该有机物属于醇,可看作是丁烷中的1个H原子被1个羟基取代产物,书写丁烷的同分异构体,根据等效氢判断丁醇的同分异构体数目;
(2)化合物C7H10O2只有3个不饱和度,而酚至少4个不饱和度,所以它的同分异构体不可能是酚,据此解答;
(3)根据所含官能团的限制书写同分异构体;
(4)根据限制条件书写同分异构体;
(5)组成为C5H10的有机物,属于烯烃的同分异构体说明含有1个碳碳双键,根据碳链缩短法书写同分异构体。
(1)分子式为C4H10O并能与金属钠反应放出氢气,则该有机物属于饱和一元醇,可看作是丁烷分子中的1个H原子被羟基取代产物,丁烷有CH3CH2CH2CH3、CH3CH(CH3)CH3两种不同结构,其中CH3CH2CH2CH3中有2种H原子,1个H原子被1个羟基取代有2种不同结构;CH3CH(CH3)CH3中有2种H原子,1个H原子被1个羟基取代也有2种不同结构,故符合条件的C4H10O结构共有2+2=4种;
(2)化合物C7H10O2的不饱和度为:![]() =3,有3个不饱和度,而酚至少4个不饱和度,所以它的同分异构体不可能是酚,故合理选项是D;
=3,有3个不饱和度,而酚至少4个不饱和度,所以它的同分异构体不可能是酚,故合理选项是D;
(3)该物质分子中含一个碳碳双键和一个羧基,含碳碳双键和羧基的同分异构体为:CH2=CHCH2COOH、CH3CH=CHCOOH;
(4)![]() 有多种同分异构体,其中属于酯类,应含酯基,能与FeCl3溶液发生显色反应,说明含有酚羟基,且苯环上有2种一硝基取代物,说明有2个不同的取代基处于对位,符合条件的同分异构体的结构简式有:
有多种同分异构体,其中属于酯类,应含酯基,能与FeCl3溶液发生显色反应,说明含有酚羟基,且苯环上有2种一硝基取代物,说明有2个不同的取代基处于对位,符合条件的同分异构体的结构简式有:![]() 、
、![]() 、
、![]() ;
;
(5)C5H10的烯烃可看作是戊烷去掉相邻2个碳原子上各1个H 原子后的物质,戊烷的同分异构体有CH3-CH2-CH2-CH2-CH3、![]() 、
、 三种不同结构;若为CH3-CH2-CH2-CH2-CH3,相应烯烃有CH2=CH-CH2-CH2-CH3、CH3-CH=CH-CH2-CH3;若为
三种不同结构;若为CH3-CH2-CH2-CH2-CH3,相应烯烃有CH2=CH-CH2-CH2-CH3、CH3-CH=CH-CH2-CH3;若为![]() ,相应烯烃有:CH2=C(CH3)CH2CH3;CH3C(CH3)=CHCH3;CH3CH(CH3)CH=CH2;若为
,相应烯烃有:CH2=C(CH3)CH2CH3;CH3C(CH3)=CHCH3;CH3CH(CH3)CH=CH2;若为 ,则没有相应烯烃,所以分子式为C5H10的烯烃共有(不包括顺反异构)2+3=5种。
,则没有相应烯烃,所以分子式为C5H10的烯烃共有(不包括顺反异构)2+3=5种。

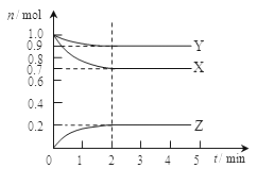
【题目】为探究![]() 、
、![]() 与盐酸(浓度为
与盐酸(浓度为![]() )反应过程中的热效应,实验测得的数据如表所示:
)反应过程中的热效应,实验测得的数据如表所示:
序号 | 35mL试剂 | 固体 | 混合前温度/℃ | 混合后温度/℃ |
① | 水 | 2.5g | 20.0 | 18.5 |
② | 水 | 3.2g | 20.0 | 24.3 |
③ | 盐酸 | 2.5g | 20.0 | 16.2 |
④ | 盐酸 | 3.2g | 20.0 | 25.1 |
由此得出的结论正确的是( )
A.![]() 固体与盐酸的反应是吸热反应
固体与盐酸的反应是吸热反应
B.![]() 固体与盐酸的反应是放热反应
固体与盐酸的反应是放热反应
C.20.0℃时,含3.2g![]() 的饱和溶液和35mL盐酸混合后的温度将低于25.1℃
的饱和溶液和35mL盐酸混合后的温度将低于25.1℃
D.20.0℃时,含2.5g![]() 的饱和溶液和35mL盐酸混合后的温度将低于16.2℃
的饱和溶液和35mL盐酸混合后的温度将低于16.2℃
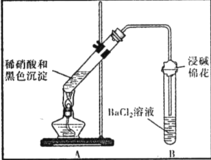
【题目】某兴趣小组对铜与浓硫酸反应产生的黑色沉淀(可能含有CuO、CuS、Cu2S,其中CuS和 Cu2S不溶于稀盐酸、稀硫酸)进行探究,实验步骤如下:
Ⅰ.将光亮铜丝插入浓硫酸,加热;
Ⅱ.待产生大量黑色沉淀和气体时,抽出铜丝,停止加热;
Ⅲ.冷却后,从反应后的混合物中分离出黑色沉淀,洗净、干燥备用。
回答下列问题:
(1)步骤Ⅱ产生气体的化学式为______________。
(2)向含微量 Cu2+试液中滴加K4[Fe(CN)6]溶液,能产生红褐色沉淀.现将少量黑色沉淀放入稀硫酸中,充分振荡以后,再滴加K4[Fe(CN)6]溶液,未见红褐色沉淀,由此所得结论是______________。
(3)为证明黑色沉淀含有铜的硫化物,进行如下实验:
装置 | 现象 | 结论及解释 |
| ①A试管中黑色沉淀逐渐溶解 | a.现象②说明黑色沉淀具有_________性。 |
(4)CuS固体能溶于热的浓硫酸,请用有关平衡移动原理加以解释:__________。
(5)为测定黑色沉淀中Cu2S 的百分含量,取0.2g 步骤Ⅰ所得黑色沉淀,在酸性溶液中用 40.0mL 0.075mol/L KMnO4溶液处理,发生反应如下:
8MnO4﹣+5Cu2S+44H+═10Cu2++5SO2↑+8Mn2++22H2O
6MnO4﹣+5CuS+28H+═5Cu2++5SO2↑+6Mn2++14H2O
反应后煮沸溶液,赶尽SO2,过量的高锰酸钾溶液恰好与35.0mL 0.1mol/L (NH4)2Fe(SO4)2溶液反应完全,则混合物中Cu2S 的质量分数为____________________。
【题目】用如图装置制取并收集气体,对应的装置和试剂均正确的是( )

Ⅲ收集气体 | Ⅰ中试剂a,b | Ⅱ中试剂c | Ⅳ中试剂d | |
A | SO2 | 稀硫酸与铜片 | 浓硫酸 | NaOH溶液 |
B | Cl2 | 浓盐酸与二氧化锰 | 饱和氯化钠溶液 | NaOH 溶液 |
C | HBr | 浓硫酸与溴化钠 | 浓硫酸 | 水 |
D | CO | 甲酸与浓硫酸 | 浓硫酸 | 酸性KMnO4溶液 |
A. AB. BC. CD. D