题目内容
某元素的原子结构示意图为 ,下列关于该元素的说法中,错误的是
,下列关于该元素的说法中,错误的是
| A.它的阳离子带3个单位正电荷 |
| B.它是一种金属元素 |
| C.它的阳离子有10个质子 |
| D.其原子核外有13个电子 |
C
解析试题分析:从原子结构示意图看出是铝原子的结构示意图,铝原子失去3个电子生成铝离子,铝离子带3个单位正电荷,A对,铝是金属元素,B对;铝离子的质子数与铝原子相同为13个,C错;从图看出原子核外有13个电子,D对。
考点:原子结构示意图和原子组成的认识。

下列气体中,可用固体NaOH干燥的是
| A.CO2 | B.Cl2 | C.HCl | D.NH3 |
下列有关物质应用的说法正确的是
| A.生石灰用作食品抗氧剂 | B.盐类都可作调味品 |
| C.铝罐可久盛食醋 | D.小苏打是面包发酵粉的主要成分之 |
轻轨电车是近年来城市发展的一种无污染的新兴交通工具,当轻轨电车开动时,轻轨电车与架空电线的接触点由于高速摩擦会产生高温,因此接触点上的材料应该具有现耐高温,不易氧化,能导电的性质,你认为接触点上的材料应选用
| A.金刚石 | B.铝 | C.石墨 | D.铜 |
下列互为同位素的是
| A.613C和C60 | B.白磷和红磷 | C.乙醇和甲醚 | D.11H和12H |
前18号元素中最外层电子数是次外层电子数一半的元素有
| A.1种 | B.2种 | C.3种 | D.4种 |
下列有关物质结构的表述正确的是( )
A.次氯酸的电子式 | B.乙烯的分子式  |
C.钠离子的结构示意图 | D.碳-12原子 126C |
(14分)某实验小组用0.50mol/L氢氧化钠溶液和0.50mol/L硫酸溶液进行反应热的测定。
Ⅰ.配制0.50mol/L氢氧化钠溶液
(1)若实验中大约要使用245mL NaOH溶液,至少需要称量NaOH固体_________克。
(2)配制过程中,所需要的玻璃仪器有_____________________________________
Ⅱ.测定稀硫酸和稀氢氧化钠溶液反应的反应热实验装置如下: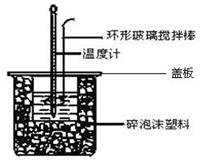
(3)如图装置中仪器环形玻璃搅拌棒作用是___________________________________;
(4)烧杯间填满碎泡沫塑料、大烧杯上加盖硬纸板的作用是__________________
(5)已知稀硫酸与稀氢氧化钠溶液发生中和反应生成1 mol水时,放出57.3 KJ热量。请写出硫酸与氢氧化钠发生中和反应的热化学方程式:__________________________________________,用0.2 mol 稀硫酸溶液与足量稀氢氧化钠溶液反应,能放出________kJ热量。
(6)在测定中和反应的反应热的实验中,下列叙述正确的是
| A.测定中和反应的反应热时,酸碱中和之后应读取体系达到的最高温度 |
| B.中和反应的试验中,应快速将NaOH溶液一次倒入盛盐酸的小烧杯中 |
| C.可以用氢氧化钾代替氢氧化钠,浓硫酸代替稀硫酸 |
| D.在测定中和反应的反应热实验中,每完成一次反应热热测定,至少需要读三次温度 |
下列盐的水溶液,其pH值小于7的是( )
| A.NH4Cl溶液 | B.NaCl溶液 | C.Na2SO4溶液 | D.NaHCO3溶液 |