题目内容
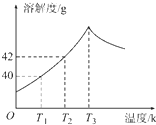 图为Na2SO4的溶解度曲线,已知硫酸钠晶体(Na2SO4?10H2O)在温度为T3K 时开始分解为无水硫酸钠.现有142g温度为T2K的饱和硫酸钠溶液,当温度降为T1K或升为T4K(T4>T3)时析出晶体的质量相等,则温度为T4K时Na2SO4的溶解度为
图为Na2SO4的溶解度曲线,已知硫酸钠晶体(Na2SO4?10H2O)在温度为T3K 时开始分解为无水硫酸钠.现有142g温度为T2K的饱和硫酸钠溶液,当温度降为T1K或升为T4K(T4>T3)时析出晶体的质量相等,则温度为T4K时Na2SO4的溶解度为
- A.小于40g
- B.等于40g
- C.等于42g
- D.大于42g
A
分析:由图知在T1时溶解度是40g,142g温度为T2K的饱和硫酸钠溶液,当温度降为T1K时,如果析出来的晶体是Na2SO4则有2g,实际应为Na2SO4?10H2O肯定要大于2g.
解答:由图知在T1时溶解度是40g,142g温度为T2K的饱和硫酸钠溶液,当温度降为T1K时,如果析出来的晶体是Na2SO4则有2g,实际应为Na2SO4?10H2O肯定要大于2g.那么在T4K时析出的晶体是无水硫酸钠,质量是大于2g.所以温度为T4K时Na2SO4的溶解度应该小于T1时的溶解度,即小于40g.
故选A.
点评:本题考查溶解度、饱和溶液的概念,对于有关溶解度的计算题,找出该温度的饱和溶液,弄清楚硫酸钠晶体(Na2SO4?10H2O)在温度为T3K 时开始分解为无水硫酸钠是解题的关键.
分析:由图知在T1时溶解度是40g,142g温度为T2K的饱和硫酸钠溶液,当温度降为T1K时,如果析出来的晶体是Na2SO4则有2g,实际应为Na2SO4?10H2O肯定要大于2g.
解答:由图知在T1时溶解度是40g,142g温度为T2K的饱和硫酸钠溶液,当温度降为T1K时,如果析出来的晶体是Na2SO4则有2g,实际应为Na2SO4?10H2O肯定要大于2g.那么在T4K时析出的晶体是无水硫酸钠,质量是大于2g.所以温度为T4K时Na2SO4的溶解度应该小于T1时的溶解度,即小于40g.
故选A.
点评:本题考查溶解度、饱和溶液的概念,对于有关溶解度的计算题,找出该温度的饱和溶液,弄清楚硫酸钠晶体(Na2SO4?10H2O)在温度为T3K 时开始分解为无水硫酸钠是解题的关键.

练习册系列答案
相关题目
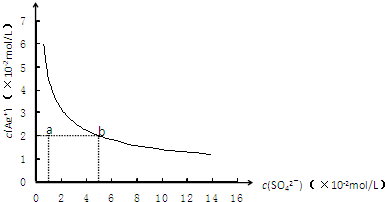

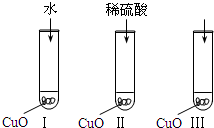 (2007?汕头二模)氧化铜是一种黑色固体,可溶于稀硫酸.某同学想知道是稀硫酸的哪种粒子(H2O,H+,SO42-)能使氧化铜溶解.请你和他一起通过如图Ⅰ、Ⅱ和Ⅲ三个实验完成这次探究活动.
(2007?汕头二模)氧化铜是一种黑色固体,可溶于稀硫酸.某同学想知道是稀硫酸的哪种粒子(H2O,H+,SO42-)能使氧化铜溶解.请你和他一起通过如图Ⅰ、Ⅱ和Ⅲ三个实验完成这次探究活动.
 8Na2CrO4+2Fe2O3+8CO2
8Na2CrO4+2Fe2O3+8CO2