题目内容
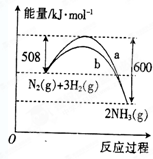
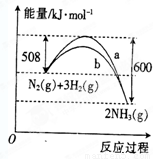
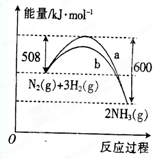 如图是某条件下N2与H2反应过程中能量变化的曲线图.根据图象判断下列叙述中正确的是( )
如图是某条件下N2与H2反应过程中能量变化的曲线图.根据图象判断下列叙述中正确的是( )分析:A、依据热化学方程式的书写原则判断,△H=放出的能量-吸收的能量;
B、根据催化剂与能耗的关系分析;
C、根据催化剂只能降低反应的活化能,不改变化学平衡分析;
D、依据热化学方程式的书写方式与能量的关系.
B、根据催化剂与能耗的关系分析;
C、根据催化剂只能降低反应的活化能,不改变化学平衡分析;
D、依据热化学方程式的书写方式与能量的关系.
解答:解:A、该反应放出的能量大于吸收的能量,所以为放热反应,热化学方程式为:N2(g)+3H2(g)=2NH3(g)△H=-92kJ?mol-1,故A错误;
B、催化剂能改变反应的路径,使发生反应所需的活化能降低,即可降低生产能耗,故B错误;
C、加入催化剂改变反应速率,不改变化学平衡,反应的热效应不变,故C错误;
D、热化学方程式为:N2(g)+3H2(g)=2NH3(g)△H=-92kJ?mol-1,则2NH3(g)=N2(g)+3H2(g)△H=+92kJ?mol-1,故D正确;
故选D.
B、催化剂能改变反应的路径,使发生反应所需的活化能降低,即可降低生产能耗,故B错误;
C、加入催化剂改变反应速率,不改变化学平衡,反应的热效应不变,故C错误;
D、热化学方程式为:N2(g)+3H2(g)=2NH3(g)△H=-92kJ?mol-1,则2NH3(g)=N2(g)+3H2(g)△H=+92kJ?mol-1,故D正确;
故选D.
点评:本题考查了热化学方程式的书写方法和要求,图象分析能力,主要是催化剂的概念,对反应影响的实质和结果.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
 氮是地球上含量丰富的元素,氮及其化合物的研究在生产、生活中有着重要意义.
氮是地球上含量丰富的元素,氮及其化合物的研究在生产、生活中有着重要意义.
 CH4(g)+HC≡CH(g)+H2(g);
△H1=156.6 kJ·mol-1
CH4(g)+HC≡CH(g)+H2(g);
△H1=156.6 kJ·mol-1