题目内容
17.下列关于化学键的说法正确的是( )| A. | 构成单质分子的微粒一定含有共价键 | |
| B. | 非极性键只存在于双原子分子中 | |
| C. | 由非金属元素组成的化合物不一定是共价化合物 | |
| D. | 不同元素组成的多原子分子里的化学键一定是极性键 |
分析 化学键是相邻的原子之间强烈的相互作用,化学键有离子键、共价键和金属键,注意并不是所有物质都含有化学键.
解答 解:A.构成单质分子的微粒不一定含有共价键,如稀有气体,故A错误;
B.非极性键可能存在多原子分子中,如乙烯,故B错误;
C.由非金属元素组成的化合物不一定是共价化合物,如铵盐,故C正确;
D.不同元素组成的多原子分子里的化学键可能含有非极性键,如C2H6中含有C-C键,为非极性键,故D错误;
故选C.
点评 本题考查了化学键和物质的关系,为高频考点,难度不大,易错选项是A,注意稀有气体是单原子分子,只存在分子间作用力,不含化学键,为易错点.

练习册系列答案
相关题目
7.中科院国家纳米科学中心2013年11月22日宣布,该中心科研人员在国际上首次“拍”到氢键的“照片”,实现了氢键的实空间成像,为“氢键的本质”这一化学界争论了80多年的问题提供了直观证据.这不仅将人类对微观世界的认识向前推进了一大步,也为在分子、原子尺度上的研究提供了更精确的方法.下列说法中正确的是( )
| A. | 氢键是自然界中最重要、存在最广泛的化学键之一 | |
| B. | 正是氢键的存在,冰能浮在水面上 | |
| C. | 由于氢键的存在,沸点:HCl>HBr>HI>HF | |
| D. | 由于氢键的存在,水分子变的更稳定了 |
8.在下列无色透明溶液中,能大量共存的离子组是( )
| A. | Cu2+、Na+、SO42-、Cl- | B. | Ca2+、NH4+、Cl-、OH- | ||
| C. | Ba2+、H+、I-、SO42- | D. | Mg2+、Na+、NH4+、NO3- |
5.当萘与H2以物质的量比为1:1发生加成反应时,与1,3-丁二烯发生1,4-加成相似的产物有( )
①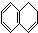 ②
② ③
③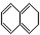 ④
④
①
 ②
② ③
③ ④
④
| A. | ①③ | B. | ②④ | C. | ②③ | D. | ①④ |
2.下列说法中错误的是( )
| A. | 需要加热才能发生的反应一定是吸热反应 | |
| B. | 化学键的断裂和形成是化学反应中能量变化的主要原因 | |
| C. | 化学反应中的能量变化通常表现为热量的变化 | |
| D. | 反应物总能量和生成物总能量的相对大小决定了反应是放出能量还是吸收能量 |
9.下列有关叙述正确的是( )
| A. | H、D、T具有相同的质子数,是氢元素的三种同位素 | |
| B. | OH-与H3O+组成元素相同,所含质子数相同 | |
| C. | 结构示意图为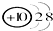 和 和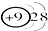 两种粒子为同一种元素 两种粒子为同一种元素 | |
| D. | 元素原子最外层电子数的多少是判断金属性和非金属性强弱的依据 |
6.NA表示阿伏加德罗常数,下列说法正确的是( )
| A. | 4.6gNO2和N2O4的混合气体中氧原子数小于0.2NA | |
| B. | 1 L 0.1 mol.L-1的Na2S溶液中离子总数小于0.3NA | |
| C. | 在标况下,2.24 L CCl4含有0.4NA个Cl原子 | |
| D. | 0.1 mol H2O2参加氧化还原反应时,不一定转移0.2NA个电子 |
1.已知aXm+和bYn-两种离子的电子层结构相同,则a等于( )
| A. | b+m+n | B. | b+m-n | C. | b-m+n | D. | b-m-n |