题目内容
今有A、B、C、D四种元素,其中A元素是1826年一位法国青年科学家发现的。他在研究海水制盐时,往剩余的副产物苦卤中通入氯气后发现溶液颜色变深,再经进一步提取,可得一种红棕色液体,有刺鼻的臭味。B、C、D均为短周期元素,D原子核内的质子数正好等于C原子核内质子数的两倍,而它们最外层电子数相等,且都具有负化合价。D原子的最内电子层上电子数则是B原子最外层电子数的2倍,且A、B、C、D四种元素均不在同一周期。则四种元素是:A ,B ,C ,D 。
解析:A的判断应由苦卤与氯反应得到红棕色液体的一段叙述得出,知其为溴。由C、D都有负价,判断它们是非金属。短周期里两非金属元素的核电荷数(质子数)是两倍关系且它们最外层电子数相同的只有O和S,因此确定出C为氧、D为硫。D最内层电子只能是K层的2个电子,它是B最外层电子数的2倍,说明B最外层只1个电子,为第ⅠA族元素,再根据四种元素处于不同周期可确定B为氢。
答案:溴 氢 氧 硫

练习册系列答案
相关题目


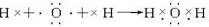



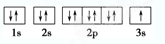
 NH4++OH-,试判断溶于水后,形成的合理结构是________。(填右图中的字母)
NH4++OH-,试判断溶于水后,形成的合理结构是________。(填右图中的字母) 