��Ŀ����
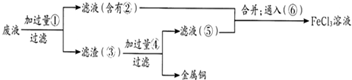
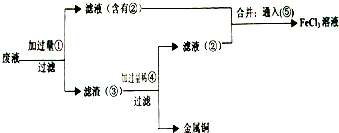
���ӹ�ҵ����30%��FeCl3��Һ��ʴ���ھ�Ե���ϵ�ͭ��������ӡˢ��·�壮
��1��������Һ��Fe3+���ڵ��Լ���
��2�����Ӹ�ʴ��ķ�Һ�л���ͭ�����»��FeCl3��Һ�������Լ��У���Ҫ�õ���һ���ǣ�����ĸ��
������ˮ�����ۢ�Ũ�����Ũ�����Ũ��ˮ����ˮ
A���ڢܢ�B���ۢܢ�C���ڢܢ�D���٢ܢ�
��3��д��FeCl3��Һ�����ͭ������Ӧ�����ӷ���ʽ
��4����ȥFeCl2�л��е�FeCl3���ɼ���
��1��������Һ��Fe3+���ڵ��Լ���
KSCN��Һ
KSCN��Һ
��֤��Fe3+���ڵ���������Һ��ΪѪ��ɫ
��Һ��ΪѪ��ɫ
��2�����Ӹ�ʴ��ķ�Һ�л���ͭ�����»��FeCl3��Һ�������Լ��У���Ҫ�õ���һ���ǣ�����ĸ��
A
A
��������ˮ�����ۢ�Ũ�����Ũ�����Ũ��ˮ����ˮ
A���ڢܢ�B���ۢܢ�C���ڢܢ�D���٢ܢ�
��3��д��FeCl3��Һ�����ͭ������Ӧ�����ӷ���ʽ
2Fe3++Cu=Cu2++2Fe2+
2Fe3++Cu=Cu2++2Fe2+
��4����ȥFeCl2�л��е�FeCl3���ɼ���
����
����
�� ��ȥFeCl3�л��е�FeCl2���ɼ���Cl2����ˮ��H2O2��O3��
Cl2����ˮ��H2O2��O3��
����Ӧ�����ӷ���ʽΪCl2+2Fe2+=2Fe3++2Cl-��H2O2+2H++2Fe2+=2Fe3++2H2O
Cl2+2Fe2+=2Fe3++2Cl-��H2O2+2H++2Fe2+=2Fe3++2H2O
����������1�����ݼ��������ӵķ���ѡ��ʹ���Լ�����Ӧ������
��2���������ù������۽�������ת����ͭ���ʣ�Ȼ������������ĵ����������ۣ��ټ�����ˮ���������ӻ�ԭ�������ӣ��ݴ�ѡ��ʹ�õ��Լ���
��3������ͭ�������ӷ�Ӧ�����������Ӻ�ͭ���ӣ��ݴ�д����Ӧ�����ӷ���ʽ��
��4�����ݳ���ԭ������������ѡ���Լ����������������������������������ӣ�ע�ⲻ�������µ����ʣ�
��2���������ù������۽�������ת����ͭ���ʣ�Ȼ������������ĵ����������ۣ��ټ�����ˮ���������ӻ�ԭ�������ӣ��ݴ�ѡ��ʹ�õ��Լ���
��3������ͭ�������ӷ�Ӧ�����������Ӻ�ͭ���ӣ��ݴ�д����Ӧ�����ӷ���ʽ��
��4�����ݳ���ԭ������������ѡ���Լ����������������������������������ӣ�ע�ⲻ�������µ����ʣ�
�����1�����������ӳ�ѡ�õ��Լ�Ϊ���軯����Һ������Һ�д��������ӣ���Һ���ɺ�ɫ�����������ӣ�
�ʴ�Ϊ��KSCN��Һ����Һ��ΪѪ��ɫ��
��2���Ӹ�ʴ��ķ�Һ�л���ͭ�����»��FeCl3��Һ�����ù������۽�������ת����ͭ���ʣ����˺�õ�����ͭ��Ȼ������������ĵ����������ۣ��ټ�����ˮ���������ӻ�ԭ�������ӣ�����ѡ�õ��Լ��У������ۡ���Ũ���ᡢ����ˮ��
��ѡA��
��3��FeCl3��Һ�����ͭ������Ӧ����ͭ�������������ӣ���Ӧ�����ӷ���ʽΪ��2Fe3++Cu=Cu2++2Fe2+��
�ʴ�Ϊ��2Fe3++Cu=Cu2++2Fe2+��
��4����ȥFeCl2�л��е�FeCl3����Ҫ�������۽������ӻ�ԭ���������Ӽ��ɣ���ȥFeCl3�л��е�FeCl2��ѡ�����������������ӻ�ԭ�������ӣ�����ʹ����ˮ��˫��ˮ������������Ӧ�����ӷ���ʽΪ��Cl2+2Fe2+=2Fe3++2Cl-��H2O2+2H++2Fe2+=2Fe3++2H2O��
�ʴ�Ϊ�����ۣ�Cl2����ˮ��H2O2��O3�ȣ�Cl2+2Fe2+=2Fe3++2Cl-��H2O2+2H++2Fe2+=2Fe3++2H2O��
�ʴ�Ϊ��KSCN��Һ����Һ��ΪѪ��ɫ��
��2���Ӹ�ʴ��ķ�Һ�л���ͭ�����»��FeCl3��Һ�����ù������۽�������ת����ͭ���ʣ����˺�õ�����ͭ��Ȼ������������ĵ����������ۣ��ټ�����ˮ���������ӻ�ԭ�������ӣ�����ѡ�õ��Լ��У������ۡ���Ũ���ᡢ����ˮ��
��ѡA��
��3��FeCl3��Һ�����ͭ������Ӧ����ͭ�������������ӣ���Ӧ�����ӷ���ʽΪ��2Fe3++Cu=Cu2++2Fe2+��
�ʴ�Ϊ��2Fe3++Cu=Cu2++2Fe2+��
��4����ȥFeCl2�л��е�FeCl3����Ҫ�������۽������ӻ�ԭ���������Ӽ��ɣ���ȥFeCl3�л��е�FeCl2��ѡ�����������������ӻ�ԭ�������ӣ�����ʹ����ˮ��˫��ˮ������������Ӧ�����ӷ���ʽΪ��Cl2+2Fe2+=2Fe3++2Cl-��H2O2+2H++2Fe2+=2Fe3++2H2O��
�ʴ�Ϊ�����ۣ�Cl2����ˮ��H2O2��O3�ȣ�Cl2+2Fe2+=2Fe3++2Cl-��H2O2+2H++2Fe2+=2Fe3++2H2O��
���������⿼���������Ӻ��������Ӽ��鷽�������������������ӵ�ת�����������е��Ѷȵ����⣬���������߿��������ǿ�������ڼ���ѧ����ѧϰ��Ȥ��ѧϰ�����ԣ�

��ϰ��ϵ�д�
�����Ŀ