��Ŀ����
��8�֣��£�N2H4���ֳ���������һ�ֿ�ȼ�Ե�Һ�壬���������ȼ�ϡ�
���µĽṹʽΪ�� ��
����ͼ��һ���绯ѧ����ʾ��ͼ��

�ٲ�Ƭ�Ϸ����ĵ缫��Ӧ�� ��
�ڼ���ʹ����һ����ȼ�ϵ����Ϊ�������еĵ�Դ��ͭƬ�������仯128g������һ����ȼ�ϵ�����������ı�״���µĿ��� L����������������������Ϊ20%����
���¡�������ȼ�ϵ����һ�ּ���ȼ�ϵ�أ���������Ⱦ�����ʡ��������Һ��20%��30%�� KOH��Һ���¡�������ȼ�ϵ�طŵ�ʱ�������ĵ缫��Ӧʽ�� ��
���𰸡�
��1�� ��2�֣�
��2�֣�
��2��N2H4 �� 4e- +4OH�� = N2 + 4H2O ��2�֣�
��Cu2+ +2e-= Cu��2�֣���112L��2�֣�
�����������ݵ��ԭ���ĵ缫��Ӧ�ص�д�������ϵĵ缫��Ӧʽ������������仯������ؼ��㣬������֪��ѧ��Դ����д����������֪ʶǨ�Ƶķ���д���µĸ�����Ӧ��

��ϰ��ϵ�д�
 ��У����ϵ�д�
��У����ϵ�д�
�����Ŀ
 �£�N2H4���ֳ���������һ�ֿ�ȼ��Һ�壬�������������ﷴӦ�������ɵ�����ˮ���������ȼ�ϣ�
�£�N2H4���ֳ���������һ�ֿ�ȼ��Һ�壬�������������ﷴӦ�������ɵ�����ˮ���������ȼ�ϣ� �£�N2H4���ֳ��������㷺���ڻ���ƽ������л��ϳɼ�ȼ�ϵ�أ�NO2�Ķ�����N2O4���ǻ���г��õ�����������ش��������⣺
�£�N2H4���ֳ��������㷺���ڻ���ƽ������л��ϳɼ�ȼ�ϵ�أ�NO2�Ķ�����N2O4���ǻ���г��õ�����������ش��������⣺
 �£�N2H4���ֳ���������һ�ֿ�ȼ��Һ�壬�������ȼ�ϣ�
�£�N2H4���ֳ���������һ�ֿ�ȼ��Һ�壬�������ȼ�ϣ�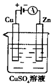 �£�N2H4���ֳ����������������ȼ�ϣ���һ����ȼ�ϵ���еĵ������Һ��20%��30%��KOH��Һ����ȼ�ϵ�ؿ���Ϊ��ͼװ���еĵ�Դ�������жϴ�����ǣ�������
�£�N2H4���ֳ����������������ȼ�ϣ���һ����ȼ�ϵ���еĵ������Һ��20%��30%��KOH��Һ����ȼ�ϵ�ؿ���Ϊ��ͼװ���еĵ�Դ�������жϴ�����ǣ�������