题目内容
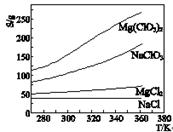
已知四种盐的溶解度(S)曲线如右图所示,下列说法不正确的是

A.将MgCl2溶液蒸干后不可能得到MgCl2固体
B.将NaCl溶液蒸干可得NaOH固体
C.NaClO3中混有少量NaCl杂质,可用重结晶法提纯
D.可用MgCl2和NaClO3制备Mg(ClO3)2
【答案】
B
【解析】
试题分析:因MgCl2能够水解,水解产生了Mg(OH)2和HCl,加热水解平衡正向移动,氯化氢易挥发,所以将MgCl2溶液蒸干可得固体为Mg(OH)2,故A错误;因NaCl不会发生水解,所以将NaCl溶液蒸干可得NaCl固体,,故B错误;NaClO3与NaCl的溶解度随温度变化差别较大,所以可以可用重结晶法提纯,故C正确;反应MgCl2+2NaClO3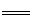 Mg(ClO3)2+2NaCl类似于侯德榜制碱法生成NaHCO3的原理,因为NaCl溶解度小而从溶液中析出,使反应向生成Mg(ClO3)2的方向进行,故D正确;
Mg(ClO3)2+2NaCl类似于侯德榜制碱法生成NaHCO3的原理,因为NaCl溶解度小而从溶液中析出,使反应向生成Mg(ClO3)2的方向进行,故D正确;
考点:考查溶解度曲线的意义及应用。

练习册系列答案
 每日10分钟口算心算速算天天练系列答案
每日10分钟口算心算速算天天练系列答案
相关题目
已知四种盐的溶解度(S)曲线如图所示,下列说法不正确的是( )
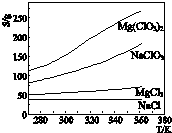

| A、将MgCl2溶液蒸干后不可能得到MgCl2固体 | B、将NaCl溶液蒸干可得NaOH固体 | C、NaClO3中混有少量NaCl杂质,可用重结晶法提纯 | D、可用MgCl2和NaClO3制备Mg(ClO3)2 |
已知四种盐的溶解度(S)曲线如右图所示,下列说法不正确的是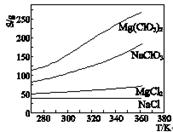
| A.将NaCl溶液蒸干可得NaCl固体 |
| B.将MgCl2溶液蒸干可得MgCl2固体 |
| C.Mg(ClO3)2中混有少量NaCl杂质,可用重结晶法提纯 |
| D.可用MgCl2和NaClO3制备Mg (ClO3)2 |
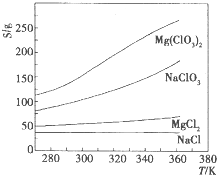 已知四种盐的溶解度(s)曲线如图所示,下列说法不正确的是( )
已知四种盐的溶解度(s)曲线如图所示,下列说法不正确的是( )