题目内容
碱性电池具有容量大、放电电流大的特点,因而得到广泛应用。锌—锰碱性电池以氢氧化钾溶液为电解液,电池总反应式为:Zn(s)+2MnO2(s)+H2O(l)==Zn(OH)2(s)+Mn2O3(s)。下列说法错误的是
A.电池工作时,锌失去电子
B.电池正极的电极反应式为:2MnO2(s)+H2O(1)+2e—=Mn2O3(s)+2OH- (aq)
C.电池工作时,电子由正极通过外电路流向负极
D.外电路中每通过0.2mol电子,锌的质量理论上减小6.5g
C
【解析】
试题分析:A、原电池工作原理是负极失电子,发生氧化反应,则根据方程式可知电池工作时,锌失去电子,故A正确;B、正极得电子,发生还原反应,所以正极的电极反应式为:2MnO2+H2O+2e-=Mn2O3+2OH-,故B正确;C、电池工作时,电子由负极流向正极,故C错误;D、由Zn(s)+2MnO2(s)+H2O(l)═Zn(OH)2(s)+Mn2O3(s)可知,反应转移电子2mol时消耗65gZn,则反应转移0.2mol电子理论上消耗6.5gZn,故D正确;故选C。
考点:考查原电池原理的应用

练习册系列答案
 作业辅导系列答案
作业辅导系列答案 同步学典一课多练系列答案
同步学典一课多练系列答案 经典密卷系列答案
经典密卷系列答案 金牌课堂练系列答案
金牌课堂练系列答案
相关题目
下列有关微粒之间关系和特征描述正确的是( )。
选项 | 微粒 | 相互关系 | 特征描述 |
A | C60、C70、C540 | 同位素 | 微粒中只含非极性共价键 |
B | 新戊烷、2,2-二甲基丙烷 | 同分异构体 | 常温常压下呈气态 |
C | 同素异形体 | 铂作氨催化氧化时的催化剂 | |
D | 甲酸、硬脂酸 | 同系物 | 能发生酯化反应 |
X 、Y、Z、W是中学化学常见的四种物质,他们之间具有如图所示转化关系,则下列组合不可能的是
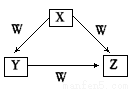
| X | Y | Z | W |
A | C | CO | CO2 | O2 |
B | Na | Na2O | Na2O2 | O2 |
C | AlCl3 | Al(OH)3 | NaAl(OH)4 | NaOH |
D | Fe | FeCl2 | FeCl3 | Cl2 |
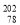
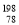
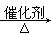 CH3CH2Br
CH3CH2Br
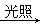 CH2Cl2+2HCl
CH2Cl2+2HCl