题目内容
某二元酸(化学式用H2A表示)在水中的电离方程式是:
H2A====H++HA- HA-![]() H++A2-
H++A2-
试完成下列问题:
(1)Na2A溶液显_______(填“酸性”“中性”或“碱性”)。
理由是___________________________________________(用离子方程式表示)。
(2)在0.1 mol·L-1的Na2A溶液中,下列粒子浓度关系式正确的是_________。
A.c(A2-)+c(HA-)+c(H2A)=0.1 mol·L-1
B.c(OH-)=c(H+)+c(HA-)
C.c(Na+)+c(H+)=c(OH-)+c(HA-)+2c(A2-)
D.c(Na+)=2c(A2-)+2c(HA-)
(3)已知0.1 mol·L-1NaHA溶液的pH=2,则0.1 mol·L-1 H2A溶液中氢离子的物质的量浓度可能是0.11 mol·L-1_________ (填“<”“>”或“=”),理由是____________________________________。
(4)0.1 mol·L-1 NaHA溶液中各种离子浓度由大到小的顺序是:__________________________。
(1)碱性 A2-+H2O![]() HA-+OH-
HA-+OH-
(2)BCD
(3)< H2A第一步电离产生的H+,抑制了HA-的电离。
(4)c(Na+)>c(HA-)>c(H+)>c(A2-)>c(OH-)
解析:
电解质溶液试题在近几年高考试卷中屡有出现,这是一道另辟蹊径,思维要求较高的题目。
第(1)问要求书写水解方程式,在书写时要求符合规范。
第(2)问:A选项只要注意到H2A第一步电离是完全的,就能判断H2A在水溶液中不存在,从而否决它。B选项实质是物料守恒式。C选项实质是电荷守恒式。D选项反映的是:
由水电离产生的c(OH-)=由水电离产生的c(H+)。
第(4)问的解答融于第(3)问的解答之中
0.1 mol·L-1 NaHA溶液:
NaHA![]() Na++HA-
Na++HA-
0.1![]() 0.1 0.1
0.1 0.1
pH=2,c(H+)=10-2 mol·L-1
HA-![]() H++A2-
H++A2-
10-2←10-2→10-2
故:c(Na+)=0.1 mol·L-1 c(HA-)=(0.1-0.01) mol·L-1,水也电离产生c(H+),故c(H+)略大于10-2 mol·L-1 c(A2-)=10-2 mol·L-1 c(OH-)=10-14/10-2 mol·L-1
可见:c(Na+)>c(HA-)>c(H+)>c(A2-)>c(OH-)
0.1 mol·L-1 H2A溶液
H2A![]() H++HA-
H++HA-
0.1→ 0.1 0.1
HA-![]() H++A2-
H++A2-
若是单独存在的0.1 mol·L-1 HA-溶液,c(H+)=10-2 mol·L-1,第一步电离产生的H+会对第二步电离产生抑制作用,故第二步电离产生的c(H+)<10-2 mol·L-1,故c总(H+)<(0.1+0.01) mol·L-1=0.11 mol·L-1 。

(Ⅰ)常温下,将某一元酸HA(甲、乙、丙、丁代表不同的一元酸)和NaOH溶液等体积混合,两种溶液的物质的量浓度和混合溶液的pH如下表所示:
| 实验编号 | HA的物质的量 浓度(mol·L-1) | NaOH的物质的量 浓度(mol·L-1) | 混合后 溶液的pH |
| 甲 | 0.1 | 0.1 | pH=a |
| 乙 | 0.12 | 0.1 | pH=7 |
| 丙 | 0.2 | 0.1 | pH>7 |
| 丁 | 0.1 | 0.1 | pH=10 |
(1)从甲组情况分析,如何判断HA是强酸还是弱酸? ▲ 。
(2)乙组混合溶液中离子浓度c(A— )和c(Na+)的大小关系是 ▲ 。
A.前者大 B. 后者大 C. 二者相等 D.无法判断
(3)从丙组实验结果分析,该混合溶液中离子浓度由大到小的顺序是 ▲ 。
(4)分析丁组实验数据,写出该混合溶液中下列算式的精确结果(列式):
c(Na+)—c(A-)= ▲ mol·L-1
(Ⅱ)某二元酸(化学式用H2B表示)在水中的电离方程式是:
![]()
![]()
回答下列问题:
(5)在0.1mol/L的Na2B溶液中,下列粒子浓度关系式正确的是 ▲ 。
A.c( B2— )+c(HB— )=0.1mol/L B.c( B2— )+ c(HB— )+c(H2B)=0.1mol/L
C c(OH— )=c(H+)+ c(HB— ) D.c(Na+)+c(OH)=c(H+)+ c(HB— )
(Ⅰ)常温下,将某一元酸HA(甲、乙、丙、丁代表不同的一元酸)和NaOH溶液等体积混合,两种溶液的物质的量浓度和混合溶液的pH如下表所示:
| 实验编号 | HA的物质的量 浓度(mol·L-1) | NaOH的物质的量 浓度(mol·L-1) | 混合后 溶液的pH |
| 甲 | 0.1 | 0.1 | pH=a |
| 乙 | 0.12 | 0.1 | pH=7 |
| 丙 | 0.2 | 0.1 | pH>7 |
| 丁 | 0.1 | 0.1 | pH=10 |
(1)从甲组情况分析,如何判断HA是强酸还是弱酸? ▲ 。
(2)乙组混合溶液中离子浓度c(A— )和c(Na+)的大小关系是 ▲ 。
A.前者大 B. 后者大 C. 二者相等 D.无法判断
(3)从丙组实验结果分析,该混合溶液中离子浓度由大到小的顺序是 ▲ 。
(4)分析丁组实验数据,写出该混合溶液中下列算式的精确结果(列式):
c(Na+)—c(A-)= ▲ mol·L-1
(Ⅱ)某二元酸(化学式用H2B表示)在水中的电离方程式是:
![]()
![]()
回答下列问题:
(5)在0.1mol/L的Na2B溶液中,下列粒子浓度关系式正确的是 ▲ 。
A.c( B2— )+c(HB— )=0.1mol/L B.c( B2— )+ c(HB— )+c(H2B)=0.1mol/L
C c(OH— )=c(H+)+ c(HB— ) D.c(Na+)+c(OH)=c(H+)+ c(HB— )
 H++A2-回答下列问题:
H++A2-回答下列问题: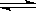 H+ +
A2- 回答下列问题:
H+ +
A2- 回答下列问题: H++A2-回答下列问题:
H++A2-回答下列问题: